
Contents
- 1 利尿薬(Diuretics)の作用メカニズムと臨床的用途の解説
- 2 1. 利尿薬の作用機序
- 3 2. 臨床的用途
- 4 3. 利尿薬療法の初期効果
- 5 4. 利尿薬使用の注意点
- 6 利尿薬(Diuretics)の作用と慢性使用時の補償的メカニズムの解説
- 7 1. 利尿薬の初期効果
- 8 2. 慢性使用時の補償的メカニズム(Compensatory Mechanisms)
- 9 3. 慢性使用の臨床的影響
- 10 4. 利尿薬の使用におけるバランス
- 11 1. 浸透圧性利尿薬(Osmotic diuretics)
- 12 2. ループ利尿薬(Loop diuretics)
- 13 3. チアジド系利尿薬(Thiazide diuretics)
- 14 4. 炭酸脱水酵素阻害薬(Carbonic anhydrase inhibitors)
- 15 5. 鉱質コルチコイド受容体拮抗薬(Mineralocorticoid receptor antagonists)
- 16 6. ナトリウムチャネル阻害薬(Sodium channel blockers)
- 17 急性腎障害(Acute Kidney Injury, AKI)の解説
- 18 1. 急性腎障害の特徴
- 19 2. 分類と成因
- 20 3. Fractional Excretion of Sodium (FeNa)
- 21 4. 臨床的評価と診断
- 22 5. 治療
- 23 急性腎不全(Acute Renal Failure, ARF)の腎前性(Pre-renal)の原因とメカニズムの解説
- 24 1. 腎前性AKIの原因(Causes of Pre-renal AKI)
- 25 2. 腎前性AKIの病態生理(Pathophysiology)
- 26 3. 腎前性AKIの特徴的所見
- 27 4. 腎前性AKIと腎性AKIの鑑別
- 28 5. 治療
- 29 1. 血液検査の特徴
- 30 2. 尿検査の特徴
- 31 3. 腎前性AKI診断のポイント
- 32 4. 腎前性AKIと腎性AKIの鑑別
- 33 腎性急性腎不全(Intrinsic Renal Failure)の解説
- 34 1. 腎性AKIの主な原因
- 35 2. 腎性AKIの臨床診断の特徴
- 36 3. 治療
- 37 急性尿細管壊死(Acute Tubular Necrosis, ATN)の解説
- 38 1. 急性尿細管壊死の原因(Causes)
- 39 2. 病態生理(Mechanism of Ischemic ATN)
- 40 3. 臨床所見と診断
- 41 4. ATNの臨床経過
- 42 5. 治療
- 43 急性尿細管壊死(Acute Tubular Necrosis, ATN):毒素や薬剤による場合の解説
- 44 1. 主な腎毒性物質(Common Toxic Agents)
- 45 2. 病態生理(Mechanism of ATN caused by Toxins or Medications)
- 46 3. 治癒と回復(Healing and Recovery)
- 47 4. 臨床的特徴
- 48 5. 治療
- 49 急性腎障害(Acute Kidney Disease, AKD)における腎後性(Post-renal Failure)の解説
- 50 1. 腎後性急性腎不全の原因
- 51 2. 病態生理(Pathophysiology)
- 52 3. 腎後性急性腎不全の診断
- 53 4. 合併症(Complications)
- 54 5. 治療(Treatment)
- 55 慢性腎臓病(Chronic Kidney Disease, CKD)の解説
- 56 1. 慢性腎臓病の病態生理
- 57 2. 慢性腎臓病の主な原因(Causes for CKD)
- 58 3. 診断基準(Criteria for Diagnosis of CKD)
- 59 4. 合併症(Complications of CKD)
- 60 5. 治療(Treatment for CKD)
- 61 慢性腎臓病(Chronic Kidney Disease, CKD)の臨床症状とそのメカニズム
- 62 1. 臨床症状(Clinical Features)
- 63 2. 症状とそのメカニズムのまとめ
- 64 3. 治療の基本戦略
- 65 慢性腎臓病(CKD)における高リン血症(Hyperphosphatemia)とその関連症状の解説
- 66 1. 高リン血症と低カルシウム血症の病態生理
- 67 2. 臨床症状
- 68 3. 診断基準
- 69 4. 治療(Treatment)
- 70 間質性腎炎(Interstitial Nephritis)の解説
- 71 1. 間質性腎炎の原因(Causes)
- 72 2. 腎盂腎炎(Pyelonephritis)
- 73 3. 病態生理(Pathophysiology)
- 74 4. 診断
- 75 5. 治療(Treatment)
- 76 6. 予後
- 77 ネフローゼ症候群(Nephrotic Syndrome)と微小変化型ネフローゼ症候群(Minimal-Change Nephrotic Syndrome, MCNS)の解説
- 78 1. 微小変化型ネフローゼ症候群の特徴
- 79 2. 病態生理(Mechanism of MCNS)
- 80 3. 臨床症状
- 81 4. 診断
- 82 5. 治療
- 83 6. 予後
利尿薬(Diuretics)の作用メカニズムと臨床的用途の解説
利尿薬(diuretics)は、腎臓でのナトリウム(sodium)や塩化物(chloride)の再吸収を抑制することで、尿量の増加(diuresis)を引き起こす薬剤です。その結果、水分(water)も尿中に排泄されるため、体液量が減少します。以下に、利尿薬の作用機序や臨床的用途、治療中の変化について詳しく解説します。
1. 利尿薬の作用機序
(1) ナトリウム・塩化物の再吸収抑制
- 利尿薬は主に腎臓の尿細管(renal tubules)でのナトリウム・塩化物の再吸収を抑制します。
- ナトリウム(Na⁺)の再吸収が抑えられると、尿中の浸透圧が上昇し、水分が引き込まれて排泄量が増加します。
- このプロセスを通じて、ナトリウム排泄(natriuresis)と利尿(diuresis)が促進されます。
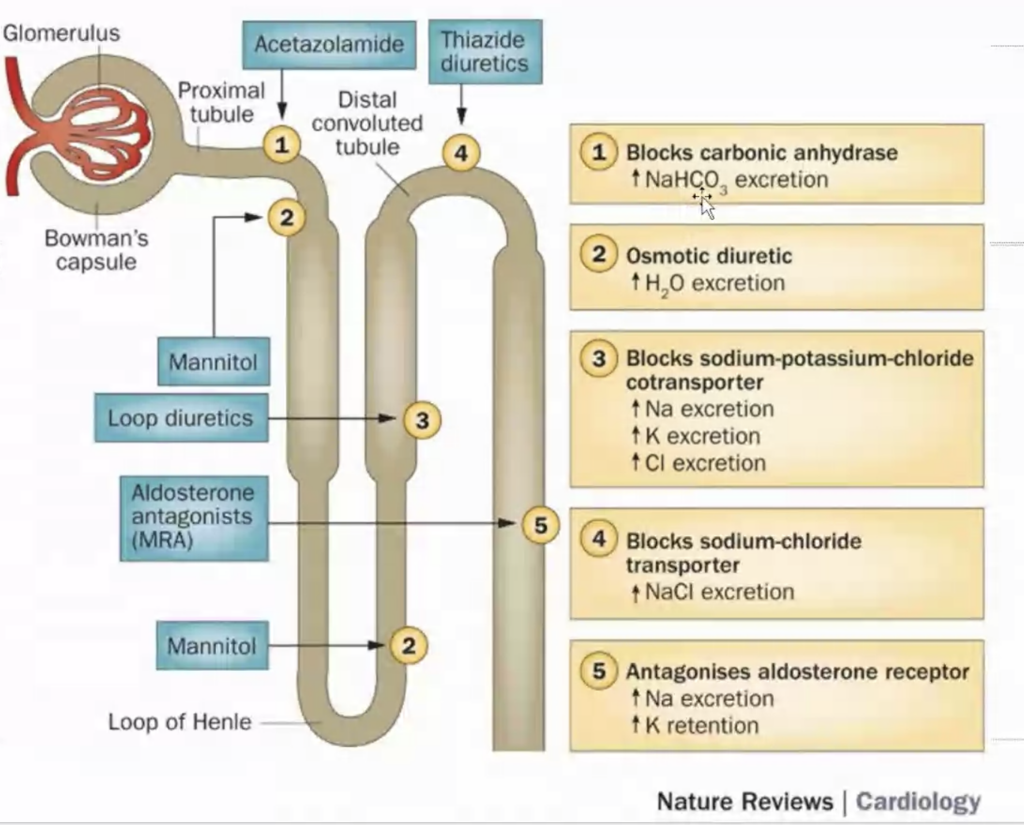
(2) 再吸収部位による作用の違い
利尿薬は作用する尿細管の部位によって効果が異なります:
- 近位尿細管(proximal tubule):炭酸脱水酵素阻害薬(例:アセタゾラミド)。
- ヘンレループ(Henle’s loop):ループ利尿薬(例:フロセミド)。
- 遠位尿細管(distal tubule):チアジド系利尿薬(例:ヒドロクロロチアジド)。
- 集合管(collecting duct):カリウム保持性利尿薬(例:スピロノラクトン、アミロライド)。
2. 臨床的用途
(1) 浮腫関連疾患の管理(Edema-related conditions)
- 浮腫は、体内に余分な水分が溜まり、組織に腫れを生じる状態です。
- 利尿薬は以下の浮腫の治療に使用されます:
- 心不全(heart failure):静脈還流の減少を助け、心臓の負担を軽減。
- 肝硬変(liver cirrhosis):腹水の減少。
- 腎疾患(renal diseases):ネフローゼ症候群や急性腎障害に伴う浮腫。
(2) 高血圧(Hypertension)の管理
- 体外へのナトリウムと水の排泄を促進し、**細胞外液量(extracellular fluid volume)**を減少させることで、血圧を低下させます。
- 特に**チアジド系利尿薬(thiazide diuretics)**は、軽度から中等度の高血圧における第一選択薬として使用されます。
3. 利尿薬療法の初期効果
(1) 尿量の急激な増加
- 利尿薬の投与直後、尿量は通常の20倍程度に増加することがあります。
- これは急速なナトリウム排泄と水分排泄によるもので、一時的に体液バランスが大きく変化します。
(2) 体液バランスの一時的な乱れ
- 利尿薬療法は、塩分と水分の摂取量と腎臓での排泄量とのバランスを一時的に崩します。
- 初期段階では血圧や体液量の急激な変化が見られることがありますが、持続的な使用により体内のバランスが再調整されます。
4. 利尿薬使用の注意点
(1) 副作用
- 電解質異常(Electrolyte imbalances):
- ナトリウム欠乏症(低ナトリウム血症)。
- カリウム欠乏症(低カリウム血症)— 特にループ利尿薬やチアジド系利尿薬で顕著。
- 脱水(Dehydration):
- 過剰な水分排泄により、血液量が低下する。
- 腎機能への影響:
- 急性腎障害(過度の体液減少による腎血流低下)。
(2) 慎重投与が必要な場合
- 高齢者、心不全患者、腎疾患を持つ患者では慎重に投与量を調整する必要があります。

利尿薬(Diuretics)の作用と慢性使用時の補償的メカニズムの解説
利尿薬は短期的には尿量の急激な増加をもたらしますが、慢性的な使用では体内の補償的なメカニズムが作動し、薬の効果に影響を与えることがあります。このメカニズムは、腎臓や循環系が体液バランスを維持しようとする反応によるものです。以下に詳しく解説します。
1. 利尿薬の初期効果
- 尿量の急増(Urine output increase):
- 投与直後、尿量は通常の最大20倍に増加します。これは、ナトリウム(sodium)と水分の再吸収が抑制されるためです。
- この急激な排泄によって、細胞外液量(extracellular fluid volume)が減少し、体液量が大幅に調整されます。
2. 慢性使用時の補償的メカニズム(Compensatory Mechanisms)
(1) 細胞外液量の減少による影響
- 利尿薬により、細胞外液量が減少します。これが持続すると、次の変化が起こります:
- 動脈圧(arterial pressure)の低下:
- 細胞外液量が減少することで、循環血液量が減少し、血圧が低下します。
- 糸球体濾過率(GFR)の低下:
- 血圧低下に伴い、腎臓への血流が減少し、糸球体濾過率が低下します。
- 動脈圧(arterial pressure)の低下:
(2) レニン-アンジオテンシン系(Renin-Angiotensin System, RAS)の活性化
- 細胞外液量や血圧の低下を感知すると、体内で以下の補償反応が起こります:
- レニン分泌の増加:
- 腎臓の傍糸球体装置(Juxtaglomerular Apparatus)がレニンを分泌します。
- アンジオテンシンIIの生成増加:
- レニンがアンジオテンシノーゲンを分解してアンジオテンシンIを生成し、さらにアンジオテンシン変換酵素(ACE)の作用でアンジオテンシンIIが生成されます。
- アルドステロン分泌の促進:
- アンジオテンシンIIは副腎皮質を刺激してアルドステロンを分泌させ、ナトリウム再吸収を促進します。
- レニン分泌の増加:
(3) ナトリウム再吸収の増加
- アルドステロンの作用により、遠位尿細管および集合管でナトリウム再吸収が増加します。
- ナトリウム再吸収が増えると水分の再吸収も促進され、細胞外液量の維持を助けます。
3. 慢性使用の臨床的影響
(1) 利尿薬耐性(Diuretic Resistance)
- 長期間使用すると、補償的なナトリウム再吸収の増加により、利尿薬の効果が減弱することがあります。
- 特に、腎疾患や心不全の患者で問題となる場合があります。
(2) レニン-アンジオテンシン系阻害薬の併用
- 利尿薬使用中に活性化するレニン-アンジオテンシン系を抑制するため、ACE阻害薬(ACE inhibitors)やARB(アンジオテンシンII受容体遮断薬)が併用されることがあります。
- これにより、アルドステロンによるナトリウム再吸収を抑え、利尿薬の効果を維持します。
(3) 電解質バランスの変化
- 長期使用により、ナトリウム排泄が増加する反面、カリウム(potassium)やマグネシウム(magnesium)の喪失も起こりやすくなります。
- これが低カリウム血症や筋力低下などの副作用を引き起こす可能性があります。
4. 利尿薬の使用におけるバランス
- 短期的効果:
- 初期の尿量増加により、体液量の減少と浮腫の改善、高血圧の軽減が期待されます。
- 長期的効果:
- 補償機構が働き、薬剤単独では効果が低下することがあるため、RAS阻害薬やカリウム保持性利尿薬などとの併用が必要になる場合があります。
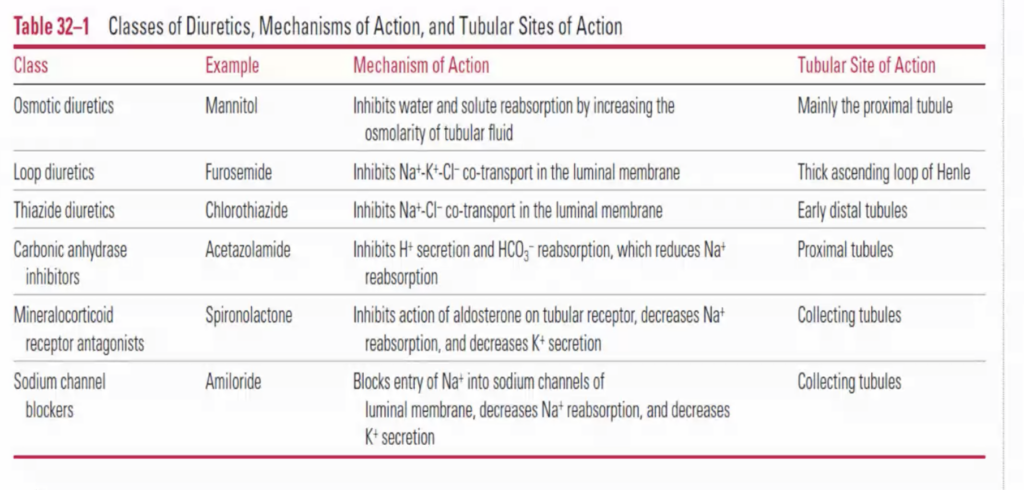
この画像は、利尿薬(diuretics)のクラス(種類)、代表的な薬剤(example)、作用機序(mechanism of action)、および**作用部位(tubular site of action)**をまとめた表です。それぞれの利尿薬の特徴について詳しく解説します。
1. 浸透圧性利尿薬(Osmotic diuretics)
- 例(Example): Mannitol(マンニトール)
- 作用機序(Mechanism of action):
- 尿細管内の浸透圧を上昇させ、水分と溶質の再吸収を抑制。
- 特に近位尿細管とヘンレループ下降脚で作用します。
- 作用部位(Tubular site of action):
- 主に近位尿細管(Proximal tubule)。
- 臨床用途:
- 脳浮腫や眼圧上昇(緑内障)に使用。
2. ループ利尿薬(Loop diuretics)
- 例(Example): Furosemide(フロセミド)
- 作用機序(Mechanism of action):
- ヘンレループ上行脚のNa⁺-K⁺-Cl⁻共輸送体を阻害。
- ナトリウム、カリウム、塩化物の再吸収を阻害し、大量の尿を排泄。
- 作用部位(Tubular site of action):
- ヘンレループ上行脚(Thick ascending loop of Henle)。
- 臨床用途:
- 浮腫(心不全、腎疾患、肝硬変)、急性肺水腫。
3. チアジド系利尿薬(Thiazide diuretics)
- 例(Example): Chlorothiazide(クロロチアジド)
- 作用機序(Mechanism of action):
- 遠位尿細管のNa⁺-Cl⁻共輸送体を阻害。
- ナトリウムと塩化物の再吸収を抑制。
- 作用部位(Tubular site of action):
- 遠位尿細管(Early distal tubules)。
- 臨床用途:
- 高血圧の第一選択薬、軽度~中等度の浮腫。
4. 炭酸脱水酵素阻害薬(Carbonic anhydrase inhibitors)
- 例(Example): Acetazolamide(アセタゾラミド)
- 作用機序(Mechanism of action):
- 炭酸脱水酵素を阻害し、H⁺の分泌とHCO₃⁻の再吸収を減少。
- ナトリウム再吸収も抑制。
- 作用部位(Tubular site of action):
- 近位尿細管(Proximal tubules)。
- 臨床用途:
- 緑内障、メタボリックアルカローシス、高山病予防。
5. 鉱質コルチコイド受容体拮抗薬(Mineralocorticoid receptor antagonists)
- 例(Example): Spironolactone(スピロノラクトン)
- 作用機序(Mechanism of action):
- アルドステロン受容体を阻害し、ナトリウム再吸収を抑制し、カリウム排泄を減少。
- 作用部位(Tubular site of action):
- 集合管(Collecting tubules)。
- 臨床用途:
- 低カリウム血症の予防、心不全、原発性アルドステロン症。
6. ナトリウムチャネル阻害薬(Sodium channel blockers)
- 例(Example): Amiloride(アミロライド)
- 作用機序(Mechanism of action):
- 集合管のナトリウムチャネルを阻害し、ナトリウムの再吸収を抑制、カリウム排泄を減少。
- 作用部位(Tubular site of action):
- 集合管(Collecting tubules)。
- 臨床用途:
- カリウム保持性利尿薬として、低カリウム血症の予防。

急性腎障害(Acute Kidney Injury, AKI)の解説
急性腎障害(AKI)は、腎機能が急速に低下する病態で、特に48時間以内に糸球体濾過率(GFR)が著しく低下することを特徴とします。腎機能低下は可逆的である場合が多く、適切な治療により回復が期待できます。
1. 急性腎障害の特徴
- 発生時間:
- 腎機能の喪失が48時間以内に起こる。
- 急速な尿量の減少(乏尿または無尿)や血中の老廃物蓄積がみられる。
- 症状と合併症:
- 尿毒症(azotemia):血液中に尿素窒素(BUN)やクレアチニンが蓄積。
- 電解質異常:高カリウム血症、代謝性アシドーシス。
- 浮腫や血圧上昇を伴う場合も。
2. 分類と成因
AKIは原因に基づいて3つの分類に分けられます:
(1) 腎前性(Prerenal AKI)
- 特徴:
- 腎臓への血流不足により発生。
- 再吸収の亢進(ナトリウム再吸収が増加)。
- 原因:
- 脱水症(severe dehydration)。
- 出血(hemorrhage)。
- 心不全(heart failure)による心拍出量の低下。
- FeNa(ナトリウム排泄率):
- 低下(< 1%):ナトリウム再吸収が活発で腎機能維持を試みるため。
(2) 腎性(Intrinsic AKI)
- 特徴:
- 腎臓の構造的損傷に起因。
- ナトリウム再吸収が低下。
- 原因:
- 急性尿細管壊死(Acute Tubular Necrosis, ATN)。
- 糸球体腎炎(glomerulonephritis)。
- 薬剤性腎障害(nephrotoxicity, e.g., NSAIDs, aminoglycosides)。
- FeNa(ナトリウム排泄率):
- 上昇(> 2%):尿細管でのナトリウム再吸収が障害されるため。
(3) 腎後性(Postrenal AKI)
- 特徴:
- 尿路の閉塞により尿が腎臓内に逆流。
- 原因:
- 前立腺肥大症(BPH)。
- 尿管結石(kidney stones)。
- 腫瘍による尿路閉塞。
- FeNa:
- 初期では正常または低下するが、進行すると腎性AKIと似たパターンを示す。
3. Fractional Excretion of Sodium (FeNa)
FeNaは、濾過されたナトリウムのうち、どの程度が尿中に排泄されるかを示す割合で、腎機能評価の指標として用いられます。
- 低いFeNa(< 1%):
- 腎前性AKIを示唆。
- 腎臓は血流低下に応じてナトリウム再吸収を増やしている。
- 高いFeNa(> 2%):
- 腎性AKIを示唆。
- 尿細管の障害によりナトリウム再吸収が減少。
- 中間値(1–2%):
- 混合型や腎後性AKIの可能性。
4. 臨床的評価と診断
- 血液検査:
- BUNとクレアチニンの上昇。
- BUN/クレアチニン比:
- 腎前性:> 20:1。
- 腎性:< 15:1。
- 尿検査:
- FeNa。
- 尿浸透圧やナトリウム濃度。
- 画像検査:
- 腎超音波:腎後性AKIの閉塞部位確認。
5. 治療
- 腎前性AKI:
- 原因治療(輸液、血流改善)。
- 腎性AKI:
- 原因となる毒性物質や薬剤の中止、腎支持療法(透析を含む)。
- 腎後性AKI:
- 尿路閉塞の解除(カテーテル挿入、結石の摘出)。

急性腎不全(Acute Renal Failure, ARF)の腎前性(Pre-renal)の原因とメカニズムの解説
急性腎不全(または急性腎障害, AKI)は、腎前性(Pre-renal)、腎性(Intrinsic)、腎後性(Post-renal)という3つの病態に分類されます。ここでは腎前性AKIについて詳しく解説します。
1. 腎前性AKIの原因(Causes of Pre-renal AKI)
腎前性AKIは、腎臓への血流量の低下に起因します。この結果、糸球体濾過率(GFR)が低下し、腎臓の機能が一時的に障害されます。
(1) 低血液量(Hypovolemia)
- 原因:
- 出血(Hemorrhage)
- 脱水症(Dehydration): 激しい発汗、下痢、嘔吐などによる。
- 過剰な利尿薬の使用。
(2) 低血圧(Hypotension)
- 原因:
- 心原性ショック(Cardiogenic shock): 心臓のポンプ機能低下による血圧低下。
- 敗血症性ショック(Septic shock): 血管の拡張と低血圧。
(3) 腎動脈の障害
- 原因:
- 腎動脈狭窄(Renal artery stenosis)
- 血管収縮薬(NSAIDsやACE阻害薬の使用)。
2. 腎前性AKIの病態生理(Pathophysiology)
(1) 腎血流量の低下
- 腎血流量が低下すると、糸球体への血液供給が減少し、**糸球体濾過率(GFR)**が低下します。
- しかし、腎臓自体は構造的に損傷を受けていないため、原因を除去すれば回復可能です。
(2) 代償機構の活性化
腎血流量の低下に対して、腎臓は以下の代償機構を活性化します:
- **レニン-アンジオテンシン-アルドステロン系(RAA系)**の活性化:
- レニンの分泌によりアンジオテンシンIIが生成され、腎動脈輸出細動脈を収縮させ、糸球体内圧を維持。
- アルドステロンによるナトリウムと水の再吸収促進。
- **抗利尿ホルモン(ADH)**の分泌:
- 集合管での水の再吸収を増加。
(3) 尿細管での尿素再吸収増加
- **近位尿細管(PCT)**では、ナトリウムと水の再吸収が増加する過程で、**尿素(BUN)**の再吸収も促進されます。
- これにより、血中尿素窒素(BUN)の濃度が著しく上昇します。
3. 腎前性AKIの特徴的所見
(1) 血液検査
- BUN/クレアチニン比の上昇(> 20:1):
- BUNが著しく上昇する一方、クレアチニン上昇は緩やか。
- 尿素が再吸収されやすい一方、クレアチニンは再吸収されにくいため。
(2) 尿検査
- 尿中ナトリウム濃度低下(< 20 mmol/L):
- ナトリウムの再吸収が亢進しているため。
- 尿浸透圧の上昇(> 500 mOsm/kg):
- 腎臓が水の再吸収を最大限に行うため。
4. 腎前性AKIと腎性AKIの鑑別
| 所見 | 腎前性AKI | 腎性AKI(急性尿細管壊死など) |
|---|---|---|
| BUN/Cr比 | 上昇(> 20:1) | 正常または軽度上昇(< 15:1) |
| 尿中Na濃度 | 低下(< 20 mmol/L) | 上昇(> 40 mmol/L) |
| 尿浸透圧 | 高い(> 500 mOsm/kg) | 低い(< 350 mOsm/kg) |
| FeNa | 低い(< 1%) | 高い(> 2%) |
5. 治療
- 腎前性AKIは原因を早期に解決することで完全に回復可能です。
(1) 脱水症や低血圧の治療
- 輸液補充(生理食塩水や乳酸リンゲル液)による循環血液量の回復。
(2) 心不全やショックの治療
- 強心薬や血管作動薬を使用して心拍出量を改善。
(3) 腎動脈狭窄の治療
- 血行再建術(ステント留置など)や血管拡張薬。
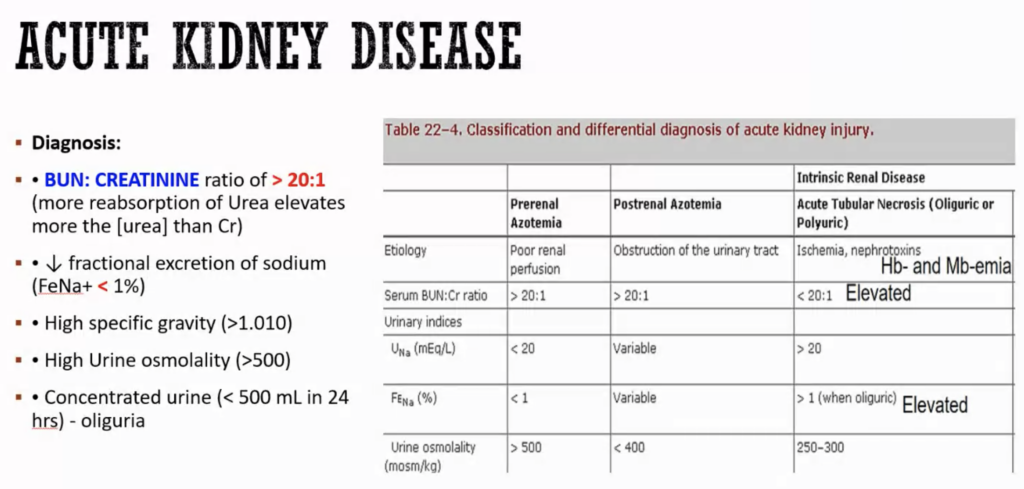
1. 血液検査の特徴
(1) BUN/クレアチニン比(BUN: Creatinine ratio)
- 基準値: > 20:1
- 理由:
- 腎血流量が低下すると、ナトリウムと水が近位尿細管で過剰に再吸収されます。
- この過程で、尿素(BUN)は容易に再吸収されますが、クレアチニン(Cr)は再吸収されにくいため、血液中でのBUNの上昇が顕著になります。
- 解釈:
- **高値(> 20:1)**は腎前性AKIを示唆します。
- **正常または低値(< 15:1)**の場合、腎性AKI(急性尿細管壊死など)を疑います。
2. 尿検査の特徴
(1) ナトリウム排泄率(Fractional Excretion of Sodium, FeNa⁺)
- 基準値: < 1%
- 理由:
- 腎血流が低下すると、腎臓はナトリウムと水を保持しようとします(RAA系とADHの作用)。
- 結果として、尿中のナトリウム排泄量が著しく減少します。
- 解釈:
- FeNa⁺ < 1% は腎前性AKIを示唆。
- FeNa⁺ > 2% は腎性AKIを示唆(尿細管がナトリウムを再吸収できない)。
(2) 尿比重(Specific Gravity)
- 基準値: > 1.010
- 理由:
- 腎臓が濃縮尿を生成しようとするため、尿比重が上昇します。
- 比重が高いほど尿が濃縮されていることを意味します。
(3) 尿浸透圧(Urine Osmolality)
- 基準値: > 500 mOsm/kg
- 理由:
- 水分再吸収が活発になり、尿中の溶質濃度が高まります。
- 高い尿浸透圧は腎前性AKIの特徴。
(4) 尿量(Urine Output)
- 基準値: < 500 mL/日(乏尿, Oliguria)
- 理由:
- 腎血流量の減少により、尿量が著しく減少します。
3. 腎前性AKI診断のポイント
以下の検査所見が腎前性AKIを支持します:
| 指標 | 基準値 | 理由 |
|---|---|---|
| BUN/Cr比 | > 20:1 | 尿素が再吸収されるが、クレアチニンはされないため。 |
| FeNa⁺(ナトリウム排泄率) | < 1% | ナトリウムが再吸収されるため排泄率が低下。 |
| 尿比重(Specific Gravity) | > 1.010 | 濃縮尿の生成による。 |
| 尿浸透圧(Urine Osmolality) | > 500 mOsm/kg | 濃縮能が保たれているため。 |
| 尿量 | < 500 mL/日(乏尿) | 腎血流量低下により尿生成が減少。 |
4. 腎前性AKIと腎性AKIの鑑別
| 指標 | 腎前性AKI | 腎性AKI(急性尿細管壊死など) |
|---|---|---|
| BUN/Cr比 | > 20:1 | < 15:1 |
| FeNa⁺ | < 1% | > 2% |
| 尿比重 | > 1.010 | < 1.010 |
| 尿浸透圧 | > 500 mOsm/kg | < 350 mOsm/kg |
| 尿中ナトリウム濃度 | < 20 mmol/L | > 40 mmol/L |

腎性急性腎不全(Intrinsic Renal Failure)の解説
腎性急性腎不全(Intrinsic Renal Failure)は、腎臓自体の構造的な損傷が原因で発生する腎障害です。損傷は主に糸球体、尿細管、または間質(interstitium)に生じます。ここでは、腎性AKIの代表的な原因とその病態について詳しく解説します。
1. 腎性AKIの主な原因
腎性AKIは、以下のような腎臓内の特定の部位が損傷を受けることによって起こります。
(a) 糸球体腎炎(Glomerulonephritis)
- 例: 溶連菌感染後糸球体腎炎(Post-Streptococcal Glomerulonephritis)
- 原因:
- 溶連菌感染(咽頭炎や皮膚感染)の後、免疫複合体が糸球体に沈着し、炎症を引き起こします。
- 病態:
- 糸球体の炎症により、糸球体濾過率(GFR)が低下し、**乏尿(oliguria)**が生じます。
- 尿中に血尿(hematuria)やタンパク尿(proteinuria)が見られることが特徴。
- 診断所見:
- 尿検査で赤血球円柱や血尿を確認。
- 血清補体(C3)が低下。
(b) 急性尿細管壊死(Acute Tubular Necrosis, ATN)
- 原因:
- 腎前性AKI(腎血流量の低下)による虚血(ischemia)。
- 腎髄質が虚血性壊死に陥ることが多い。
- 病態:
- 虚血や毒性物質により尿細管上皮細胞が損傷。
- 損傷した尿細管細胞が剥がれ落ち、尿細管内腔に「キャスト(casts)」として蓄積。
- ナトリウムや水の再吸収が著しく低下し、尿が希薄化。
- 診断所見:
- 尿検査で顆粒円柱(granular casts)や上皮細胞円柱(epithelial cell casts)。
- FeNa > 2%(ナトリウム再吸収が減少)。
- 尿浸透圧が低下(< 350 mOsm/kg)。
(c) 薬剤性腎障害(Drug-Induced Nephrotoxicity)
- 原因:
- **アミノグリコシド系抗生物質(Aminoglycosides)**などの腎毒性薬剤。
- 他にも、シスプラチンや造影剤なども腎毒性を引き起こすことがあります。
- 病態:
- 薬剤が尿細管上皮細胞に直接毒性を与える。
- 結果として尿細管の再吸収機能が障害され、尿中に老廃物や電解質が増加。
(d) 血管内溶血や横紋筋融解症(Hemolysis and Rhabdomyolysis)
- 原因:
- 血管内溶血(Hemolysis):
- 赤血球が破壊され、遊離ヘモグロビン(Hb)が血中に放出される。
- 横紋筋融解症(Rhabdomyolysis):
- 筋細胞が破壊され、筋肉タンパク質であるミオグロビン(myoglobin)が血中に放出される。
- 血管内溶血(Hemolysis):
- 病態:
- ヘモグロビンやミオグロビンは腎糸球体で濾過されるが、近位尿細管で再吸収される際に活性酸素(ROS)を生成し、尿細管細胞に損傷を与える。
- ミオグロビンは尿細管内で沈着し、尿細管閉塞を引き起こすこともある。
- 診断所見:
- 溶血では血清遊離ヘモグロビンの上昇。
- 横紋筋融解症では血清クレアチンキナーゼ(CK)の著しい上昇。
- 尿が茶褐色(ヘモグロビン尿またはミオグロビン尿)。
2. 腎性AKIの臨床診断の特徴
腎性AKIの診断には、血液検査や尿検査が重要です。
| 検査項目 | 所見 |
|---|---|
| 尿検査 | 顆粒円柱、上皮細胞円柱(急性尿細管壊死の場合) |
| BUN/クレアチニン比 | 通常 < 15:1 |
| FeNa | > 2% (ナトリウム再吸収が障害される) |
| 尿浸透圧 | < 350 mOsm/kg (尿細管の濃縮機能低下) |
| 血液検査 | 高カリウム血症(hyperkalemia)、代謝性アシドーシス(metabolic acidosis) |
| 特定の診断マーカー | CK上昇(横紋筋融解症)、低補体(糸球体腎炎) |
3. 治療
腎性AKIの治療は原因に応じて異なりますが、一般的な方針は以下の通りです:
- 原因の除去:
- 腎毒性薬剤の中止。
- 血液溶血や筋損傷の治療(輸液、利尿薬を用いたミオグロビンの排泄促進)。
- 腎支持療法:
- 高カリウム血症やアシドーシスへの対応(透析が必要な場合もある)。
- 炎症の管理(糸球体腎炎の場合):
- ステロイドや免疫抑制薬の使用。


急性尿細管壊死(Acute Tubular Necrosis, ATN)の解説
急性尿細管壊死(ATN)は、腎臓内の尿細管上皮細胞の損傷または壊死による**腎性急性腎障害(intrarenal AKI)**の主要な原因です。この状態は、腎臓の血流低下(虚血)または有害物質への曝露が原因で発生します。
1. 急性尿細管壊死の原因(Causes)
(1) 重度の虚血(Severe Ischemia)
- 機序:
- 腎臓への酸素供給不足や栄養不足により、尿細管上皮細胞が損傷。
- 主に循環血液量低下(hypovolemia)や低血圧により引き起こされる。
- 原因:
- 循環性ショック(Circulatory shock):
- 出血性ショック、敗血症性ショック、心原性ショック。
- 腎血流低下:
- 腎動脈狭窄、腎血栓症。
- 循環性ショック(Circulatory shock):
(2) 有害物質への曝露(Exposure to Harmful Agents)
- 機序:
- 毒素や薬剤が直接尿細管上皮細胞を傷害。
- 原因:
- 毒素:
- 重金属(鉛、カドミウム)、有機溶剤。
- 薬剤性:
- アミノグリコシド系抗生物質(例:ゲンタマイシン)。
- 造影剤、シスプラチン、NSAIDs。
- 筋肉壊死に伴う毒素:
- 横紋筋融解症によるミオグロビン蓄積。
- 毒素:
2. 病態生理(Mechanism of Ischemic ATN)
- 虚血による細胞損傷:
- 腎臓の血流低下により、酸素供給が不足。
- 尿細管上皮細胞がエネルギー欠乏(ATP不足)に陥り、細胞死(壊死)を引き起こす。
- 剥がれた細胞による閉塞(Tubular Blockages):
- 損傷した尿細管上皮細胞が尿細管腔に剥離して蓄積し、閉塞を引き起こす。
- 閉塞により、尿が糸球体から流れ出せなくなる(尿細管の流出阻害)。
- 腎機能の停止:
- 閉塞したネフロンでは尿が生成されず、その領域の腎機能が停止。
- 閉塞が解消されるまで、尿の流出が再開されない。
- 回復期(Recovery Phase)でも遅延する尿生成:
- 腎血流が回復しても、尿細管閉塞や上皮細胞の修復に時間がかかるため、尿量が即座に正常に戻らない。
3. 臨床所見と診断
(1) 尿検査
- 顆粒円柱(Granular casts):
- 損傷した尿細管上皮細胞や細胞残骸が形成。
- ナトリウム排泄率(FeNa):
- FeNa > 2%(尿細管でのナトリウム再吸収が障害されているため)。
- 尿浸透圧:
- < 350 mOsm/kg(尿濃縮能力が低下している)。
(2) 血液検査
- BUN/クレアチニン比(BUN:Cr ratio):
- < 15:1(腎前性AKIより低い)。
- 電解質異常:
- 高カリウム血症、代謝性アシドーシス。
(3) 尿量(Oliguria or Anuria)
- 乏尿(< 400 mL/日)または無尿。
4. ATNの臨床経過
急性尿細管壊死の経過は通常3段階に分けられます:
- 初期相(Initiation Phase):
- 損傷が発生し始める段階。
- 腎血流低下や毒性物質の暴露が引き金となる。
- 維持相(Maintenance Phase):
- 乏尿または無尿の状態が持続。
- 電解質異常や代謝性アシドーシスが顕著。
- 数日から数週間続く。
- 回復相(Recovery Phase):
- 尿細管上皮細胞の修復が始まり、尿量が増加(多尿期)。
- 腎機能が徐々に回復する。
5. 治療
(1) 原因の除去
- 血流回復:
- 血液量補正(輸液や輸血)、血圧の維持(血管作動薬の使用)。
- 毒素除去:
- 腎毒性薬剤の中止。
- 横紋筋融解症では輸液でミオグロビンを希釈して排泄促進。
(2) 腎支持療法
- 電解質管理(高カリウム血症、アシドーシスの是正)。
- 乏尿が持続する場合、透析を考慮。
(3) 回復期の管理
- 過剰な体液排泄を防ぐため、輸液量を慎重に調整。


急性尿細管壊死(Acute Tubular Necrosis, ATN):毒素や薬剤による場合の解説
急性尿細管壊死(ATN)は、毒素や薬剤による尿細管上皮細胞の直接的な損傷が原因で発生する腎性急性腎障害(Intrinsic AKI)の一種です。このタイプのATNは、腎毒性物質や薬剤の曝露に関連しており、その病態生理や予後は、損傷の範囲や基底膜の状態によって異なります。
1. 主な腎毒性物質(Common Toxic Agents)
(1) 化学物質
- 四塩化炭素(Carbon tetrachloride):
- 工業用溶剤。腎毒性に加え、肝毒性も引き起こす。
- 重金属(Heavy metals):
- 例:水銀(mercury)、鉛(lead)。
- 尿細管上皮細胞に直接的な毒性を示す。
(2) 化学薬品
- エチレングリコール(Ethylene glycol):
- 不凍液の成分。代謝産物(シュウ酸塩)が尿細管に沈着し、結晶を形成して閉塞を引き起こす。
(3) 農薬
- 殺虫剤(Insecticides):
- 含有成分が尿細管細胞に毒性を示す。
(4) 薬剤
- 抗生物質(Antibiotics):
- 例:テトラサイクリン系(tetracyclines)。
- 腎毒性を引き起こす抗生物質。
- 抗がん剤(Chemotherapy drugs):
- 例:シスプラチン(cis-platinum)。
- 尿細管細胞に直接毒性を及ぼす。
2. 病態生理(Mechanism of ATN caused by Toxins or Medications)
(1) 毒性作用
- 腎毒性物質や薬剤が尿細管上皮細胞に蓄積し、直接的な毒性作用を発揮。
- 酸化ストレスやミトコンドリアの機能障害を引き起こし、細胞死(アポトーシスまたは壊死)を誘発。
(2) 細胞剥離と閉塞
- 損傷を受けた尿細管上皮細胞が剥がれ落ち、尿細管内腔を閉塞。
- 閉塞により、尿の流出が障害され、糸球体からの濾過がさらに低下。
(3) 基底膜への損傷
- 重症例では、基底膜が破壊されることもある。
- 基底膜が破壊されると、上皮細胞の再生が妨げられ、長期的な腎障害のリスクが増加。
3. 治癒と回復(Healing and Recovery)
(1) 基底膜が保持されている場合(Intact Basement Membrane)
- 再生可能性:
- 残存する基底膜上で新しい上皮細胞が再生。
- 機能回復は通常10~20日以内に達成される。
- 予後:
- 比較的良好で、完全回復が期待される。
(2) 基底膜が破壊されている場合(Destroyed Basement Membrane)
- 再生困難:
- 基底膜が失われると細胞再生が著しく障害され、尿細管の機能回復が困難。
- 予後:
- 腎障害が長期化、または不可逆的な腎不全に進行する可能性がある。
4. 臨床的特徴
(1) 尿検査
- 顆粒円柱(Granular casts):
- 剥がれた上皮細胞とタンパク質からなる。
- 尿浸透圧低下:
- 尿濃縮能が障害され、尿浸透圧は低下(< 350 mOsm/kg)。
- FeNaの上昇:
- FeNa > 2%(ナトリウム再吸収が障害されるため)。
(2) 血液検査
- BUN/クレアチニン比低下:
- < 15:1(尿細管での尿素再吸収が障害されるため)。
- 高カリウム血症:
- カリウム排泄が低下。
5. 治療
(1) 原因物質の除去
- 腎毒性薬剤の中止(例:抗がん剤、造影剤)。
- エチレングリコールや重金属中毒では特異的な解毒剤の使用(例:フォメピゾール、キレート療法)。
(2) 電解質異常の管理
- 高カリウム血症や代謝性アシドーシスの治療。
- 重症例では一時的な透析が必要。
(3) 水分補正と腎支持療法
- 過剰な水分負荷を避けながら輸液を行い、腎血流を維持。

急性腎障害(Acute Kidney Disease, AKD)における腎後性(Post-renal Failure)の解説
腎後性急性腎不全(Post-renal Failure)は、尿路系の閉塞により尿の排泄が阻害され、腎機能が低下する病態です。適切な治療を行えば可逆的な場合が多いですが、放置すると不可逆的な腎損傷に進展する可能性があります。
1. 腎後性急性腎不全の原因
(1) 良性前立腺肥大症(Benign Prostatic Hyperplasia, BPH)
- 原因:
- 高齢男性に多く見られ、前立腺の肥大により尿道が圧迫される。
- 影響:
- 膀胱から尿を排出する流れが妨げられ、尿の逆流が発生。
(2) 尿路結石(Nephrolithiasis, Kidney Stones)
- 原因:
- 腎臓や膀胱内の結石による物理的閉塞。
- 影響:
- 結石が尿管や膀胱を塞ぎ、尿の排泄を妨害。
(3) 腎腫瘍や尿路腫瘍
- 原因:
- 腎臓や膀胱内の悪性腫瘍(renal malignancy)による尿路閉塞。
- 影響:
- 腫瘍が尿路を圧迫または閉塞する。
2. 病態生理(Pathophysiology)
(1) 尿路閉塞による腎機能低下
- 尿が腎盂や尿管で逆流し、腎内圧(腎盂内圧, PBS)が上昇。
- 糸球体濾過圧(GFR)の低下:
- 腎内圧の上昇により糸球体濾過が妨げられ、GFRが低下する。
- 長期的な閉塞では腎臓の構造的損傷(腎水腫や腎実質の萎縮)が進行。
(2) 二次的合併症
- 代謝性アシドーシス(Metabolic Acidosis):
- 腎臓が酸排泄を行えなくなるため、血中の酸性物質が蓄積。
- 電解質異常(Electrolyte Imbalances):
- 高カリウム血症、低ナトリウム血症など。
- 循環血液量異常(TECF: Total Extracellular Fluid Imbalance):
- 低血圧、浮腫。
3. 腎後性急性腎不全の診断
(1) 尿量低下(Oliguria)
- 基準:
- 尿量 < 0.5 mL/kg/時が6時間以上続く。
- 解釈:
- 尿量減少は、閉塞の初期症状として重要。
(2) 血液検査
- 急激なBUNおよび血清クレアチニンの上昇:
- 数時間から数日で著明に上昇。
- 腎後性障害に特徴的な増加パターン。
(3) 画像検査
- 腎超音波(Renal Ultrasound):
- 腎水腫(hydronephrosis)や尿路閉塞の確認に有用。
(4) 尿検査
- 初期では尿中ナトリウム排泄率(FeNa)が低下することもあるが、進行すると上昇。
- 尿中異常は明確でない場合も。
4. 合併症(Complications)
(1) 代謝性アシドーシス(Metabolic Acidosis)
- 腎臓が酸の排泄を行えず、血液が酸性化する。
- 症状として倦怠感、息切れが見られる。
(2) 高カリウム血症(Hyperkalemia)
- カリウム排泄が低下することで血中濃度が上昇。
- 重篤な場合、不整脈のリスクがある。
(3) 浮腫および低血圧
- 電解質異常や体液貯留により、血圧調節や循環が障害される。
5. 治療(Treatment)
(1) 原因の除去
- 尿路閉塞の解除:
- カテーテル挿入:
- 前立腺肥大症や膀胱閉塞の緊急対応として使用。
- 結石の除去:
- 衝撃波破砕術(ESWL)や内視鏡手術。
- 腫瘍の治療:
- 外科的切除または化学療法。
- カテーテル挿入:
(2) 合併症の管理
- 代謝性アシドーシス:
- 重炭酸ナトリウム(NaHCO₃)の投与で是正。
- 高カリウム血症:
- 除細動薬(カルシウム製剤)、カリウム排泄促進剤(ケイキサレート)を使用。
- 浮腫や体液異常:
- 利尿薬の適切な使用。
(3) 腎支持療法
- 腎機能が回復しない場合、一時的に透析を行う。

慢性腎臓病(Chronic Kidney Disease, CKD)の解説
慢性腎臓病(CKD)は、数か月から数年にわたり腎機能が徐々に低下する進行性の病態です。不可逆的な腎単位(ネフロン)の損傷と喪失が特徴で、最終的には**末期腎不全(End-Stage Renal Disease, ESRD)**に至る可能性があります。
1. 慢性腎臓病の病態生理
(1) 腎単位の喪失(Loss of Nephrons)
- 腎機能が低下する主な理由は、ネフロンの機能的喪失です。
- 機能を失ったネフロンは回復せず、腎機能は不可逆的に低下します。
(2) 補償的メカニズム(Compensatory Mechanisms)
- 残存するネフロンは、失われた機能を補うために過剰に働きます。
- 以下の補償反応が見られます:
- 糸球体内圧(PG)の増加:腎血流量の上昇により濾過を促進。
- 過剰濾過(Hyperfiltration):残存ネフロンでの濾過が増加。
- 結果:
- 過剰な作業負荷(workload)はネフロンにさらなるストレスを与え、**線維化や瘢痕形成(fibrosis, scarring)**を促進し、追加のネフロンが失われる。
2. 慢性腎臓病の主な原因(Causes for CKD)
(1) 糖尿病(Diabetes Mellitus)(最も一般的な原因)
- 機序:
- 糖尿病性腎症では、高血糖が糸球体の基底膜や血管構造に損傷を与える。
- 糸球体過剰濾過と蛋白尿を特徴とする。
- 臨床所見:
- 持続的な蛋白尿、進行する腎機能低下。
(2) 高血圧(Hypertension)
- 機序:
- 持続的な高血圧は腎血管の硬化や狭窄を引き起こし、糸球体へのダメージを蓄積。
- 臨床所見:
- 線維化、腎硬化症。
(3) 糸球体腎炎(Glomerulonephritis)
- 機序:
- 炎症による糸球体構造の破壊が進行し、蛋白尿や血尿が持続。
- 臨床所見:
- 顕著な血尿、蛋白尿、GFRの低下。
3. 診断基準(Criteria for Diagnosis of CKD)
(1) GFR(糸球体濾過率)
- 基準値: GFR < 60 mL/min/1.73m²が3か月以上持続。
- 正常GFR: 約120 mL/min/1.73m²。
- GFRの低下は腎機能低下を反映。
(2) 血清クレアチニン(Serum Creatinine)の上昇
- 特徴:
- 数か月から数年をかけて徐々に上昇。
- 腎機能が50%以上失われると血清クレアチニン濃度が目立つ。
(3) 尿検査
- 蛋白尿(Proteinuria):
- 尿中のアルブミンやタンパク質が検出される。
- 持続性蛋白尿は腎機能障害の早期指標。
- 血尿(Hematuria):
- 尿中の赤血球が確認される場合がある(糸球体腎炎に特徴的)。
4. 合併症(Complications of CKD)
(1) 電解質異常
- 高カリウム血症(Hyperkalemia):心不全や不整脈のリスク。
- 低ナトリウム血症(Hyponatremia):浮腫やけいれん。
(2) 代謝性アシドーシス
- 腎臓が酸排泄を行えず、血液が酸性化。
(3) 貧血(Anemia)
- 腎臓でのエリスロポエチン(EPO)産生低下により赤血球数が減少。
(4) 骨ミネラル異常(Renal Osteodystrophy)
- 活性型ビタミンDの減少と高リン血症により、骨密度が低下。
5. 治療(Treatment for CKD)
(1) 原因疾患の管理
- 糖尿病:
- 血糖コントロール(HbA1cを7%未満に維持)。
- ACE阻害薬またはARBによる糸球体内圧低下。
- 高血圧:
- 目標血圧:< 130/80 mmHg。
- 降圧薬の使用(特にRAA系阻害薬)。
(2) 食事療法
- 低ナトリウム食:
- 浮腫や高血圧の予防。
- 低タンパク質食:
- 尿素窒素の負担軽減。
- カリウム制限:
- 高カリウム血症の予防。
(3) 貧血治療
- エリスロポエチン製剤:
- 貧血を是正し、全身の酸素供給を改善。
(4) 腎代替療法(Renal Replacement Therapy, RRT)
- 透析(Dialysis):
- 腎機能が著しく低下した場合(GFR < 15 mL/min/1.73m²)。
- 腎移植(Kidney Transplant):
- 末期腎不全の最終治療法。

慢性腎臓病(Chronic Kidney Disease, CKD)の臨床症状とそのメカニズム
慢性腎臓病(CKD)は腎機能の不可逆的な低下を特徴とし、多様な全身症状を引き起こします。以下に主要な臨床症状とその背景にある病態生理を詳しく解説します。
1. 臨床症状(Clinical Features)
(1) 血中尿素窒素(BUN)とクレアチニンの上昇
- 原因:
- 腎臓の濾過能力が低下すると、尿素窒素(BUN)やクレアチニンが血中に蓄積します。
- 結果:
- 尿毒症(Uremia)として知られる症候群を引き起こし、疲労感、吐き気、意識障害などの症状を呈します。
(2) 高血圧(Hypertension)
- 原因:
- 腎臓での**レニン-アンジオテンシン-アルドステロン系(RAAS)**の活性化。
- 糸球体濾過率(GFR)の低下により腎血流が減少 → レニン分泌の増加。
- アンジオテンシンIIの作用で血管が収縮し、血圧が上昇。
- ナトリウムと水の排泄障害による体液量の増加も寄与。
- 腎臓での**レニン-アンジオテンシン-アルドステロン系(RAAS)**の活性化。
- 結果:
- 高血圧は腎臓のさらなる損傷を加速する悪循環を形成。
(3) ナトリウムと水の排泄障害
- 原因:
- 腎機能低下により、ナトリウムと水の排泄が正常に行えない。
- 初期ではナトリウム喪失が目立つが、後期ではナトリウムと水の貯留が優勢に。
- 結果:
- 浮腫や肺水腫の原因となる。
- 水の貯留は低ナトリウム血症(希釈性低ナトリウム血症)を引き起こす場合がある。
(4) 代謝性アシドーシス(Metabolic Acidosis)
- 原因:
- 腎臓が酸性代謝産物(固定酸:硫酸、リン酸など)を排泄できなくなる。
- 重炭酸イオン(HCO₃⁻)の再吸収が低下し、血液の酸性化が進行。
- 結果:
- 倦怠感、呼吸促進(クスマウル呼吸)などの症状を引き起こす。
(5) 高カリウム血症(Hyperkalemia)
- 原因:
- 腎臓のカリウム(K⁺)排泄能力が低下するため。
- 代謝性アシドーシス時には、細胞外液中のH⁺濃度が上昇し、細胞内からK⁺が細胞外へ移動する。
- 結果:
- 高カリウム血症は心不全や致死的な不整脈のリスクを増加させる。
(6) 貧血(Anemia)
- 原因:
- 腎臓の間質細胞で産生されるエリスロポエチン(Erythropoietin)の分泌低下。
- エリスロポエチンの減少により赤血球の産生が抑制される。
- 結果:
- 持続的な貧血が見られ、倦怠感、集中力低下、息切れなどを引き起こす。
2. 症状とそのメカニズムのまとめ
| 臨床症状 | 原因 | 結果 |
|---|---|---|
| BUNとクレアチニンの上昇 | 腎臓の濾過機能低下により老廃物が蓄積 | 尿毒症症状(吐き気、疲労、意識障害)。 |
| 高血圧 | RAASの活性化とナトリウム・水の貯留 | 血圧上昇 → 腎機能のさらなる低下。 |
| ナトリウムと水の排泄障害 | 腎臓の排泄能力低下 | 浮腫、肺水腫、希釈性低ナトリウム血症。 |
| 代謝性アシドーシス | 固定酸の排泄障害、HCO₃⁻の低下 | 血液の酸性化、倦怠感、呼吸促進。 |
| 高カリウム血症 | カリウム排泄低下、H⁺とK⁺の細胞間シフト | 致死的な不整脈、心停止のリスク。 |
| 貧血 | 腎臓でのエリスロポエチン産生低下 | 倦怠感、息切れ、持続的貧血。 |
3. 治療の基本戦略
(1) 原因疾患の管理
- 糖尿病や高血圧の厳格な管理(血糖コントロール、降圧薬の使用)。
- ACE阻害薬やARBでRAASを抑制。
(2) 症状への対処
- 高カリウム血症:
- 除細動薬(カルシウム製剤)、カリウム吸着剤(ポリスチレンスルホン酸)。
- 代謝性アシドーシス:
- 重炭酸ナトリウム(NaHCO₃)の投与で是正。
- 貧血:
- エリスロポエチン製剤と鉄剤の併用。
(3) 食事療法
- 低ナトリウム、低タンパク質、低カリウム食の実施。
- 水分摂取制限(浮腫や水中毒予防のため)。
(4) 腎代替療法(RRT)
- 透析(血液透析または腹膜透析)。
- 腎移植(根本的な治療法)。

慢性腎臓病(CKD)における高リン血症(Hyperphosphatemia)とその関連症状の解説
慢性腎臓病(CKD)では、腎機能低下によりリン(PO₄³⁻)の排泄が障害され、高リン血症が発生します。この状態は、低カルシウム血症(hypocalcemia)や二次性副甲状腺機能亢進症(secondary hyperparathyroidism)などの一連の代謝異常を引き起こし、骨の健康や全身の代謝に重大な影響を与えます。
1. 高リン血症と低カルシウム血症の病態生理
(1) 高リン血症(Hyperphosphatemia)
- 原因:
- CKDでは腎臓がリンを十分に排泄できないため、血中リン濃度が上昇。
- 影響:
- カルシウム(Ca²⁺)との結合:
- リンが細胞外液(ECF)でカルシウムと結合し、溶解性の低いリン酸カルシウムを形成。
- これにより、血清カルシウム濃度が低下(低カルシウム血症)。
- カルシウム(Ca²⁺)との結合:
(2) ビタミンD活性化障害
- 原因:
- 腎臓で**1α-ヒドロキシラーゼ(1α-hydroxylase)が不足し、ビタミンDがその活性型である1,25-ジヒドロキシコレカルシフェロール(Calcitriol)**に変換されない。
- 影響:
- 活性型ビタミンDが低下すると、腸管でのカルシウム吸収が減少し、低カルシウム血症が悪化。
(3) 二次性副甲状腺機能亢進症(Secondary Hyperparathyroidism, SHPT)
- 原因:
- 低カルシウム血症が副甲状腺を刺激し、副甲状腺ホルモン(PTH)分泌が増加。
- 影響:
- 骨リモデリングの異常:
- PTHが過剰分泌されても血清カルシウム濃度は十分に上昇せず、骨からカルシウムが過剰に放出される。
- **骨軟化症(osteomalacia)やくる病(rickets)**を引き起こす。
- 骨リモデリングの異常:
2. 臨床症状
(1) 高リン血症
- 症状:
- 初期には無症状のことが多いが、進行すると血管や軟部組織の石灰化を引き起こす。
- 動脈硬化や皮膚の石灰沈着によるかゆみ。
(2) 低カルシウム血症
- 症状:
- 筋肉のけいれん、テタニー(tetany)。
- 感覚異常や不整脈。
(3) 二次性副甲状腺機能亢進症
- 症状:
- 骨痛、骨折リスクの増加。
- 骨の変形や筋力低下。
3. 診断基準
| 指標 | 基準値の変化 | 理由 |
|---|---|---|
| 血清リン(PO₄³⁻) | 上昇(高リン血症) | 腎排泄障害により蓄積。 |
| 血清カルシウム(Ca²⁺) | 低下(低カルシウム血症) | 高リン血症とビタミンD活性化障害が原因。 |
| 活性型ビタミンD(Calcitriol) | 低下 | 腎での1α-ヒドロキシラーゼ活性低下。 |
| 副甲状腺ホルモン(PTH) | 上昇(二次性副甲状腺機能亢進症) | 低カルシウム血症による副甲状腺刺激。 |
4. 治療(Treatment)
(1) 原因の治療
- 高リン血症の管理:
- リン結合薬(Phosphate binders):
- リン酸カルシウム、炭酸ランタン、セベラマーなどを用い、食事からのリン吸収を抑制。
- 低リン食:
- 食事中のリン摂取を制限(乳製品、加工食品の制限)。
- リン結合薬(Phosphate binders):
(2) 活性型ビタミンD補充
- **活性型ビタミンD(Calcitriol)**またはその誘導体を使用。
- 腸管でのカルシウム吸収を促進し、低カルシウム血症と副甲状腺の過剰刺激を抑える。
(3) 副甲状腺の制御
- カルシウム感知受容体作動薬(Calcimimetics):
- 副甲状腺のカルシウム感知受容体に作用し、PTH分泌を抑制。
- 外科的治療:
- 重症例では副甲状腺摘出術(parathyroidectomy)。
(4) 骨代謝異常の予防
- 骨密度低下を予防し、骨折リスクを低減。
(5) 腎代替療法
- 透析(Dialysis):
- 血中リン濃度の低下に有効。
- 腎移植(Renal Transplantation):
- 根本的な治療法。

間質性腎炎(Interstitial Nephritis)の解説
間質性腎炎(Interstitial Nephritis)は、腎臓の間質組織(腎間質)に炎症や損傷が生じる疾患であり、腎構造の一次的または二次的な障害が原因となります。この病態は放置すると腎機能障害や慢性腎疾患(CKD)につながる可能性があります。
1. 間質性腎炎の原因(Causes)
(1) 二次的な損傷(Secondary Damage)
- 他の腎構造(血管、糸球体、尿細管)の損傷が腎間質の炎症を引き起こす。
- 例:
- 糸球体腎炎に伴う腎間質の損傷。
- 尿細管壊死(ATN)による炎症。
(2) 一次的な損傷(Primary Damage)
- 毒素、薬剤、または細菌感染の直接的な影響で腎間質が傷害を受ける。
- 原因:
- 毒素:重金属、化学物質。
- 薬剤:抗生物質(ペニシリン、セファロスポリン)、NSAIDs(非ステロイド性抗炎症薬)。
- 細菌感染:腎盂腎炎(pyelonephritis)。
2. 腎盂腎炎(Pyelonephritis)
腎盂腎炎は、腎間質性腎炎の一種で、細菌感染が原因で腎間質や腎盂が炎症を起こします。
(1) 主な病原体
- 大腸菌(Escherichia coli, E. coli):
- 最も一般的な病原菌で、糞便から尿路を通じて腎臓に到達します。
- その他の病原体:
- プロテウス属(Proteus)、クレブシエラ属(Klebsiella)、腸球菌(Enterococcus)など。
(2) 感染経路
- 上行性感染(Ascending Route)
- メカニズム:
- 細菌が下部尿路(膀胱、尿道)から尿管を経由して腎臓に到達。
- リスク要因:
- 尿路閉塞、逆流性尿路感染(vesicoureteral reflux)、カテーテル使用。
- メカニズム:
- 血行性感染(Hematogenous Route)
- メカニズム:
- 血流を介して腎臓に細菌が到達。
- リスク要因:
- 敗血症、細菌性心内膜炎。
- メカニズム:
(3) 症状
- 高熱、悪寒。
- 側腹部痛(腎部の痛み)。
- 頻尿、排尿時痛(下部尿路感染を伴う場合)。
- 尿中に白血球(膿尿)や細菌が検出される。
3. 病態生理(Pathophysiology)
(1) 炎症による損傷
- 炎症が腎間質に広がると、ネフロンが損傷を受ける。
- 炎症が長期化すると、腎線維化が進行し、不可逆的な腎機能低下に至る。
(2) ネフロン機能の低下
- 尿濃縮障害:
- 腎間質が損傷すると、尿濃縮メカニズムが障害され、希薄尿が形成される。
- GFRの低下:
- 糸球体への血流が減少し、濾過能力が低下。
4. 診断
(1) 尿検査
- 膿尿(pyuria):白血球が尿中に検出される。
- 細菌尿(bacteriuria):尿培養で病原菌を同定。
- 尿円柱(WBC casts):腎盂腎炎の特徴。
(2) 血液検査
- 白血球増加(leukocytosis):炎症を示唆。
- CRP/ESRの上昇:急性炎症マーカー。
(3) 画像検査
- 腎超音波:
- 腎盂拡張や膿瘍の有無を確認。
- CTスキャン:
- 深刻な感染や腎膿瘍の評価に使用。
5. 治療(Treatment)
(1) 感染症の治療
- 抗菌薬:
- 尿培養結果に基づいた感受性のある抗菌薬を使用。
- 初期治療としてフルオロキノロン(例:シプロフロキサシン)やセファロスポリンを使用することが一般的。
(2) 尿路閉塞の解除
- 原因の治療:
- 結石や腫瘍による閉塞がある場合は外科的介入が必要。
(3) 炎症の抑制
- NSAIDsの慎重な使用:
- 炎症を抑えるが、腎毒性に注意。
(4) 腎機能サポート
- 重症例では、一時的な透析が必要となる場合がある。
6. 予後
- 適切に治療された場合、急性間質性腎炎や腎盂腎炎は完全回復が期待されます。
- 遅延治療や再発の場合、慢性腎疾患(CKD)へ進行するリスクがあるため、早期診断と治療が重要です。

ネフローゼ症候群(Nephrotic Syndrome)と微小変化型ネフローゼ症候群(Minimal-Change Nephrotic Syndrome, MCNS)の解説
ネフローゼ症候群は、糸球体膜の損傷により尿中への過剰なタンパク質排泄(蛋白尿)を特徴とする病態です。この中でも、微小変化型ネフローゼ症候群(MCNS)は、小児に最も多く見られるタイプであり、光学顕微鏡では糸球体の明らかな異常が見られないことが特徴です。
1. 微小変化型ネフローゼ症候群の特徴
(1) 病理所見
- 光学顕微鏡(Light Microscopy):
- 糸球体には最小限の変化または目立った異常が見られない。
- 電子顕微鏡(Electron Microscopy):
- 足細胞(podocyte)の突起消失(foot process effacement)が確認される。
(2) 糸球体膜の損傷
- 糸球体の基底膜(glomerular basement membrane, GBM)や足細胞の機能障害により、選択的なタンパク質漏出が発生。
- 特にアルブミンが尿中に大量に漏出。
2. 病態生理(Mechanism of MCNS)
(1) 糸球体膜の損傷
- 原因:
- 免疫系の異常や細胞性免疫(T細胞の活性化)が関与していると考えられている。
- 結果:
- 糸球体膜の透過性が増加し、血漿タンパク質が尿中に漏出。
(2) タンパク質バランスの破綻
- 大量の蛋白尿(> 3.5 g/日)により、以下の変化が見られる:
- 低アルブミン血症(Hypoalbuminemia):
- 血漿タンパク濃度が低下。
- 浮腫(Edema):
- 血漿膠質浸透圧の低下により、組織間液が蓄積。
- 高脂血症(Hyperlipidemia):
- 肝臓がタンパク質低下を補うためリポタンパクを過剰産生。
- 易感染性(Susceptibility to Infections):
- 免疫グロブリンの尿中喪失により免疫機能が低下。
- 低アルブミン血症(Hypoalbuminemia):
3. 臨床症状
(1) 蛋白尿(Proteinuria)
- 尿中に選択的にアルブミンが漏出(選択的蛋白尿)。
(2) 浮腫(Edema)
- 特に顔面や下肢に目立つ。
- 重症例では腹水や胸水を伴うこともある。
(3) 低アルブミン血症(Hypoalbuminemia)
- 血清アルブミン濃度 < 3.0 g/dL。
(4) 高脂血症(Hyperlipidemia)
- 血清コレステロールやトリグリセリドの上昇。
(5) 尿検査所見
- 尿に大量のタンパク質が検出される(尿中蛋白 > 3.5 g/日)。
- 尿沈渣に脂肪円柱や卵円形脂肪体(Maltese cross appearance)。
4. 診断
(1) 臨床診断
- 主要所見:蛋白尿、低アルブミン血症、浮腫、高脂血症。
- 子どもでは臨床症状と尿検査で診断が確定することが多い。
(2) 生検
- 光学顕微鏡では異常が見られず、電子顕微鏡で足細胞の突起消失を確認。
5. 治療
(1) ステロイド療法
- 第一選択:
- **プレドニゾロン(Prednisolone)**が投与される。
- 多くの患者はステロイド感受性を示し、迅速に蛋白尿が消失。
(2) 免疫抑制薬
- ステロイド抵抗性や頻回再発例では、**シクロスポリン(Cyclosporine)やタクロリムス(Tacrolimus)**が使用される。
(3) 対症療法
- 浮腫の管理:
- 利尿薬(フロセミドなど)を使用。
- 高脂血症の管理:
- スタチン(HMG-CoA還元酵素阻害薬)の使用。
(4) 感染予防
- 易感染性があるため、感染予防が重要。
6. 予後
- 微小変化型ネフローゼ症候群は、適切な治療により良好な予後を示すことが多い。
- ステロイド感受性が高いが、頻回再発の可能性があるため長期的なフォローアップが必要。


コメント