循環系
循環系は血液中に含まれる血球や物質を全身の組織に送り届け、循環させるシステムです。血液とリンパ系血管系の両方を含み、成人の血管の全長は10万~15万kmと推定されています。血管系、または心血管系 (cardiovascular system) は次の構造から成り立っています。
- 心臓 (Heart) は血液を循環系に送り出します。
- 動脈 (Arteries) は心臓から離れる方向に血液を運ぶ血管で、分岐しながら各臓器へと細くなり、組織へ血液を届けます。
- 毛細血管 (Capillaries) は最も細い血管であり、酸素 (O₂)、二酸化炭素 (CO₂)、栄養分、老廃物が血液と組織の間で交換される場所です。毛細血管は、これに血液を送り出す小動脈や血液を集める小静脈とともに、ほぼ全ての臓器で複雑な網目状の細い管である微小血管系 (microvascular bed) を形成します。
- 静脈 (Veins) は小静脈が合流して大きくなる管で、心臓に向かって血液を運び、再びポンプで送り出される準備をします。
図11-1に示されるように、動脈、微小血管系、静脈は大きく2つに分けられます。肺循環 (pulmonary circulation) では肺で血液が酸素化され、体循環 (systemic circulation) では血液が栄養を運び、体中の組織で老廃物を除去します。
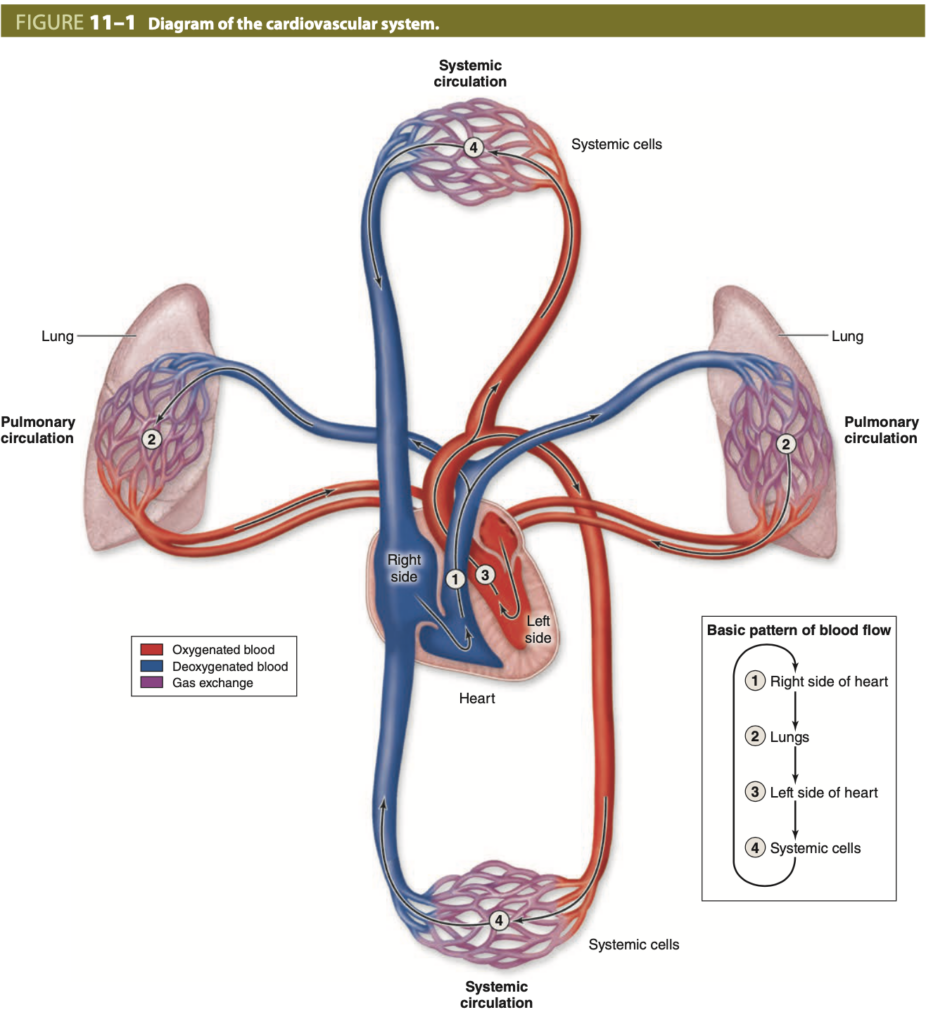
循環系(Circulatory System)
心臓、動脈、静脈、微小血管床から成るシステムは、肺循環 (pulmonary circulation) と体循環 (systemic circulation) として組織されています。肺循環では、右心室が血液を肺の血管を通じて送り出し、肺で酸素を取り込み、左心室に戻します。より大きな体循環は、左心室から血液を頭部や腕、下半身に供給し、右心室に戻します。体が安静にしているとき、血液の約70%は体循環を通じて流れ、約18%は肺循環を通じ、約12%は心臓を通過します。
リンパ系血管系 (lymphatic vascular system) は第5章で説明された組織間液に関連しており、リンパ毛細血管から始まります。リンパ毛細血管は薄い壁を持ち、閉じた端を持つ管で、組織間の液体であるリンパを運びます。これらは次第に大きくなる血管へと合流し、最終的に血管系に接続され、心臓付近の大静脈へと流れ込みます。これにより、体全体の組織空間からの液体が血液に戻ります。
血液およびリンパ系の全ての構成要素の内面は、単層扁平上皮 (simple squamous epithelium) である内皮 (endothelium) で覆われています。内皮細胞は血液と臓器の間のインターフェースとして、重要な生理学的および医学的役割を果たします。内皮細胞は選択的透過性と抗血栓性 (antithrombogenic) バリアを維持し、白血球がどこで循環から離れるかを決定し、血管の拡張や収縮、周囲細胞の成長を制御するパラクリン因子を分泌します。
心臓 (Heart)
心臓の4つの心室を構成する心筋 (cardiac muscle) は規則的に収縮し、循環系に血液を送り出します (図11-2)。右心室 (right ventricle) と左心室 (left ventricle) はそれぞれ肺循環 (pulmonary circulation) と体循環 (systemic circulation) に血液を送り出し、右心房 (right atrium) と左心房 (left atrium) はそれぞれ体と肺静脈から血液を受け取ります。心臓の壁は、内膜 (endocardium)、中膜 (myocardium)、外膜 (epicardium) の3つの主要な層で構成されています。
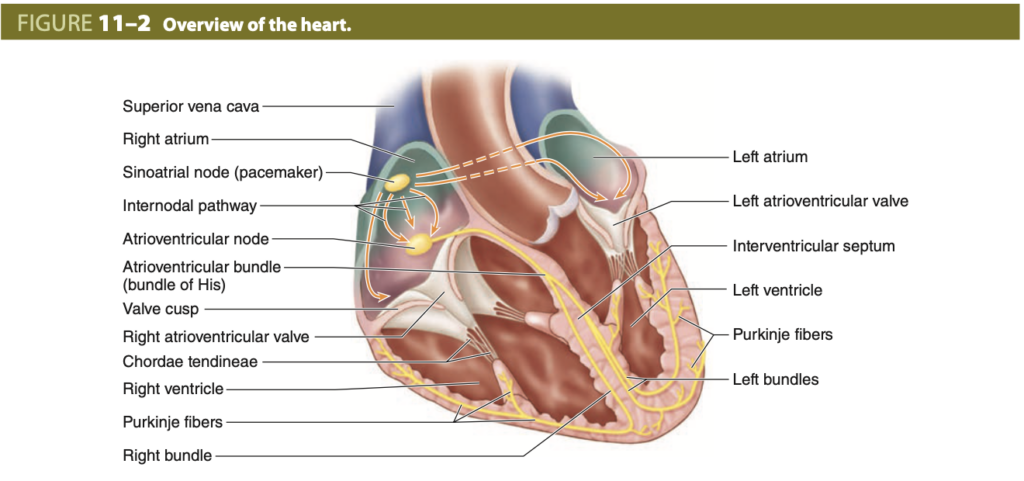
図で示されているように、ヒトの心臓には2つの心房と2つの心室があります。心室の壁の心筋 (myocardium) は心房よりも厚くなっています。心臓の弁は基本的に、密な結合組織 (dense connective tissue) でできた弁尖があり、これは心臓の結合組織(心臓骨格 (cardiac skeleton))に固定されています。この線維組織には、房室弁 (atrioventricular valves) の弁尖から伸びる腱索 (chordae tendineae) が含まれており、これらは乳頭筋 (papillary muscles) に付着しており、心室収縮時に弁が反転するのを防ぎます。弁と腱索は非血栓性の内皮 (nonthrombogenic endothelium) に覆われています。
黄色で示されているのは、心臓の電気的刺激(心拍)の伝導を開始し、心室の心筋に広がる心臓伝導系 (cardiac conducting system) の一部です。右心房の壁にある洞房結節 (SA node, 洞結節、ペースメーカー) と右心房の床にある房室結節 (AV node) は、周囲の心筋と組織学的に区別が難しい心筋組織で構成されています。AV結節は、心筋線維の特殊な束である房室束 (AV bundle, His束) と連続しており、心臓の頂部 (apex) に向かう右脚および左脚に分岐します。頂部でこれらの束はさらに細分化され、心室の心筋に広がるプルキンエ線維 (Purkinje fibers) となります。
- 内膜 (endocardium) は、内皮とそれを支える線維弾性結合組織 (fibroelastic connective tissue) の層で、その中には散在する平滑筋線維があります。深部には結合組織層があり、これは心筋と連続しており、心臓のインパルス伝導系 (impulse conducting system) を構成する修飾された心筋線維を含んでいます (図11-3)。
- 中膜 (myocardium) は主に収縮性の心筋線維からなり、各心室を螺旋状に取り囲んでいます。血液を肺循環と体循環に強く送り出すため、心室壁、特に左心室壁では中膜が厚くなっています (図11-3)。
- 外膜 (epicardium) は、血管と神経を含む疎性結合組織で支えられた単層扁平上皮 (simple squamous mesothelium) から成り立っています (図11-4)。外膜は心膜 (pericardium) の内臓層 (visceral layer) に対応し、心臓の周囲を取り囲む膜です。
心臓の大血管が出入りする場所では、外膜 (epicardium) は心膜の壁側層 (parietal layer) として反転し、心膜を裏打ちしています。心臓の動きの際、外膜の脂肪組織が下にある構造をクッションとして保護し、漿膜性の上皮細胞 (serous mesothelial cells) によって両層から分泌される潤滑液 (lubricant fluid) により心膜内での摩擦が防がれます。
これらの主要層の中で、心臓は血液を送り出す全体的な機能を果たすために重要な他の構造も含んでいます。密な不規則結合組織 (dense irregular connective tissue) から成る心臓の線維性骨格 (fibrous cardiac skeleton) は、心房と心室の筋肉を分離し、心室中隔 (interventricular septum) と心房中隔 (interatrial septum) の一部を形成し、弁尖 (valve cusps) とそれに付着する腱索 (chordae tendineae) に伸びています (図11-2および11-5)。心臓の骨格のさまざまな部分は次の機能を持ちます:
- 全ての心臓弁 (heart valves) を取り囲み、支え、固定すること
- 心房および心室の心筋 (cardiac muscle) のための確固たる挿入点を提供すること
- 心房と心室の間の電気絶縁体として機能し、心拍 (heartbeat) を調整すること
内膜下層 (subendocardial layer) と隣接する中膜には、心臓のインパルス伝導系 (impulse conducting system) を構成する修飾された心筋細胞 (modified cardiac muscle cells) が存在し、脱分極 (depolarization) の波を発生させ、隣接する心筋線維 (myocardial fibers) の規則的な収縮を刺激します。この伝導系 (conducting system) は、右心房の壁にある2つの特殊な心筋組織の節から成り、洞房結節 (sinoatrial node, SA node) と房室結節 (atrioventricular node, AV node) から成ります。
洞房結節 (SA node) は、右心房壁の上大静脈 (superior vena cava) 近くに位置する6~7 mm²の領域で、他の収縮性心筋線維よりもサイズが小さく、筋原線維 (myofibrils) が少なく、介在板 (intercalated discs) も少ない細胞で構成されています。
これらの細胞で発生したインパルスは、両心房の心筋線維に沿って移動し、その収縮を刺激します。インパルスが房室弁 (AV valve) 近くの右心房の底部に位置するやや小さい房室結節 (AV node) に達すると、そこにある心筋細胞が脱分極されます。房室結節からは房室束 (AV bundle, bundle of His) が出て、心臓の骨格内の開口部を通過し、心室中隔 (interventricular septum) に入り、左右の束に分岐します。
心臓の尖端 (apex) では、これらの束がさらに細かく分岐し、通常プルキンエ線維 (Purkinje fibers) と呼ばれる心筋線維から成る内膜下伝導網 (subendocardial conducting network) を形成します。これらの線維は淡染性で、隣接する収縮性線維よりも大きく、少ない数の周辺筋原線維と多量のグリコーゲン (glycogen) を含んでいます (図11-3)。プルキンエ線維は両心室の収縮性筋線維と遠位で交わり、両心室で同時に収縮の波を引き起こします。
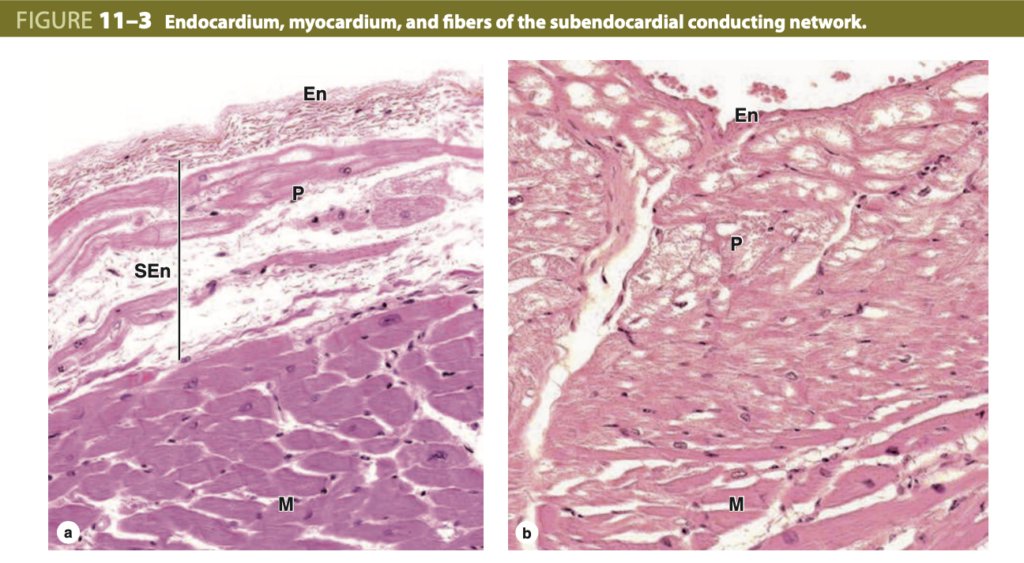
心臓の内膜 (Endocardium) 心臓の内膜は、表面の内皮 (endothelium)、それを支える線維弾性結合組織 (fibroelastic connective tissue)、および心筋の伝導に特化した心筋を取り囲む深部結合組織の層から成り、しばしば内膜下層 (subendocardial layer) と呼ばれ、心筋の結合組織と連続しています。 (a) 心室の内膜下層 (subendocardial layer) は、心臓の伝導ネットワークに属するプルキンエ線維 (Purkinje fibers) を取り囲んでいます。これらは収縮よりもインパルスの伝導に特化した修飾された心筋線維であり、介在板 (intercalated disks) で接合されています。プルキンエ線維はグリコーゲンを含みますが、細胞小器官が少なく、筋原線維 (myofibrils) は周辺部にわずかしか存在しないため、収縮性の筋線維 (contractile muscle fibers) よりも淡く染色されます。 (b) 心房の壁では、伝導を行うプルキンエ様線維 (Purkinje-like fibers) がしばしば内膜下層の大部分を占め、内皮 (endothelium) に近い場所に位置し、心筋の収縮性線維と融合しています。
心臓には副交感神経系 (parasympathetic) と交感神経系 (sympathetic) の神経成分が両方とも支配しています。神経節 (ganglia) の神経細胞および神経線維は洞房結節 (SA node) と房室結節 (AV node) の近くにあり、運動や感情的ストレスの際に心拍数やリズムに影響を与えます。副交感神経系 (迷走神経, vagus nerve) の刺激は心拍を遅くし、一方で交感神経系の刺激はペースメーカー (pacemaker) の活動を加速させます。心筋線維の間には自由神経終末 (free nerve endings) が存在し、痛みを感知します。例えば、部分的に閉塞した冠動脈 (coronary arteries) が局所的な酸素不足を引き起こした場合に生じる狭心症 (angina pectoris) などです。
医学的応用 (Medical Application)
心臓弁 (heart valves) の構造異常は、発育上の欠陥、特定の感染症後の瘢痕形成、または高血圧 (hypertension) などの心血管疾患によって引き起こされることがあります。このような異常な弁はきちんと閉じず、わずかな血液の逆流 (regurgitation) を許し、これが心雑音 (heart murmur) と呼ばれる異常な心音を引き起こします。弁の欠陥が重度の場合、心臓は通常の血液量を循環させるためにより多くの労力を要し、その結果、増加した作業量に対応するために心臓が肥大します。欠陥のある心臓弁は、外科手術で修復されるか、大型動物のドナーからの弁や人工弁 (artificial valve) に置き換えられることがよくあります。これらの弁の置換は完全な内皮被覆 (endothelial covering) がないため、患者はこれらの部位での血栓形成 (thrombus formation) を防ぐために外因性の抗凝固剤 (anticoagulant agents) を必要とします。
血管壁の組織
すべての血管(毛細血管を除く)の壁には、内皮に加えて平滑筋と結合組織が含まれています。これらの組織の量や配置は、主に血圧などの機械的要因や、組織の局所的な代謝的ニーズによって影響を受けます。内皮は、血液と組織間液という2つの主要な内部コンパートメントの間で半透膜の役割を果たす特殊な上皮です。血管内皮細胞は、血流に沿った方向に長軸があり、扁平で多角形、かつ細長い形状をしています。内皮は基底膜 (basal lamina) とともに、分子の双方向の交換を単純拡散や能動輸送、受容体介在性エンドサイトーシス (receptor-mediated endocytosis)、トランスサイトーシス (transcytosis) などのメカニズムで媒介・監視します(これについては第4章で説明されています)。
血液と組織の間の代謝物交換における重要な役割に加えて、内皮細胞には他にもいくつかの機能があります:
- 内皮 (endothelium) は非血栓性 (nonthrombogenic) の表面を提供し、血液が凝固しないようにし、局所的な血栓形成を制御する物質(ヘパリン (heparin)、組織プラスミノーゲン活性化因子 (tissue plasminogen activator, tPA)、フォンウィレブランド因子 (von Willebrand factor) など)を分泌します。
- 細胞は局所的な血管の緊張や血流を調節し、平滑筋の収縮(エンドセリン-1 (endothelin-1)、アンジオテンシン変換酵素 (angiotensin-converting enzyme, ACE) など)や弛緩(一酸化窒素 (nitric oxide, NO)、プロスタサイクリン (prostacyclin) など)を刺激するさまざまな因子を分泌します。
- 内皮 は炎症 (inflammation) や局所的な免疫応答においていくつかの役割を果たします。静脈内の内皮細胞は、傷害や感染部位で特定の白血球 (white blood cells) が停止し、経内皮移行 (transendothelial migration) を行うことを誘導します。このような状況下では、Weibel-Palade 小体と呼ばれる独特の細長い顆粒が細胞膜と融合することで、Pセレクチン (P-selectin) が迅速にルーメン表面に発現します。第12章でさらに詳述されるように、セレクチンへの接着は、白血球が必要な場所で活性化される最初のステップです。また、内皮細胞は炎症中に局所的な白血球の活動に影響を与えるさまざまなインターロイキン (interleukins) も分泌します。
- 様々な条件下で、内皮細胞は特定の白血球系統の増殖や血管壁を構成する細胞の増殖を促進するたんぱく質を含む成長因子 (growth factors) を分泌します。血管内皮増殖因子 (vascular endothelial growth factor, VEGF) などの成長因子は、胚発生中の間葉から血管系を形成する血管新生 (vasculogenesis) を刺激し、成人において血管を維持し、正常な成長、組織修復、再生、および腫瘍など病的状態における毛細血管の発芽と成長を促進します。
血管新生 (angiogenesis) においては、他の成長因子であるアンジオポエチン (angiopoietins) が内皮細胞を刺激し、平滑筋細胞 (smooth muscle cells) や線維芽細胞 (fibroblasts) を動員して血管壁の他の組織を形成させます。
医学的応用 (Medical Application)
正常な血管内皮 (vascular endothelium) は非血栓性 (antithrombogenic) であり、血液細胞や血小板が付着することを防ぎ、血栓形成を阻止します。微小血管の内皮細胞が組織損傷によって損傷すると、基底膜下の組織にあるコラーゲン (collagen) が露出し、血小板 (platelets) の凝集を誘発します。これらの血小板は、血漿中のフィブリノーゲン (fibrinogen) からフィブリン (fibrin) を生成する一連のイベントを引き起こす因子を放出します。これにより、血管内での血栓 (thrombus) が形成され、損傷した血管からの出血を止める役割を果たします。
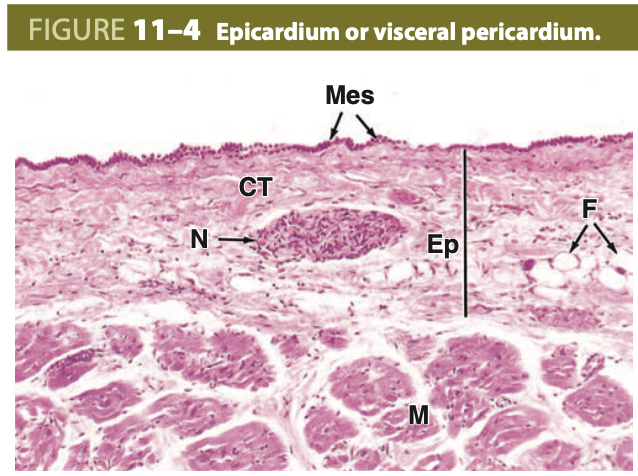
心外膜 (Epicardium)
心臓の外層である心外膜 (epicardium) は冠動脈 (coronary vessels) の場所であり、かなりの量の脂肪組織 (adipose tissue) を含んでいます。この断面では、心房の一部の心筋 (myocardium) と心外膜 (epicardium) が見られます。心外膜は、疎性結合組織 (loose connective tissue) で構成されており、自律神経 (autonomic nerves) と変動する量の脂肪組織を含んでいます。心外膜は心膜の臓側層 (visceral layer of the pericardium) に相当し、単層の中皮 (mesothelium) によって覆われ、心膜腔 (pericardial cavity) の反対側にある壁側心膜 (parietal pericardium) に接触する際の摩擦を防ぐ潤滑液を分泌します。
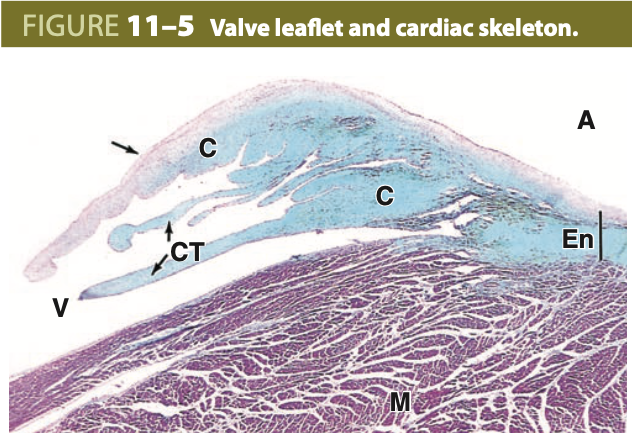
心臓の線維性骨格 (Fibrous Cardiac Skeleton)
心臓の線維性骨格は、密な不規則結合組織で構成されており、心臓弁 (heart valves) を固定し、2つの房室管 (atrioventricular canals) を取り囲んでその形状を保ちます。写真では、房室弁の弁尖の断面と、それに付着する腱索 (chordae tendineae) が見られます。これらの構造は、主に密な結合組織 (dense connective tissue) で構成され、薄い内皮層 (endothelium) に覆われています。弁のコラーゲン豊富な結合組織は淡青色に染色されており、弁の基部にある線維環 (fibrous ring) の結合組織と連続しています。
大きな血栓からは、塞栓 (emboli, 単数形: embolus) と呼ばれる固形物が血流に乗って離れ、遠くの血管を閉塞する可能性があります。どちらの場合も、血流が遮断され、生命を脅かす状況を引き起こす可能性があります。そのため、内皮層の完全性が重要であり、血小板と基底膜下の結合組織との接触を防ぐことが抗血栓性機構の一環となります。
血栓形成に関連する疾患の初期段階、例えば心筋梗塞 (myocardial infarct) や脳卒中 (stroke)、または肺塞栓症 (pulmonary embolism) などの場合、患者は静脈内で組織プラスミノーゲン活性化因子 (tPA, tissue plasminogen activator) を投与されます。tPAはセリンプロテアーゼ (serine protease) であり、フィブリンを分解して血栓を迅速に溶解します。
平滑筋線維は、毛細血管より大きいすべての血管の壁に存在し、層状に螺旋状に配置されています。小動脈や細動脈では、平滑筋細胞は多くのギャップ結合 (gap junctions) によって接続されており、血管収縮 (vasoconstriction) と血管拡張 (vasodilation) が可能です。これらは、全体的な血圧の調節において重要な役割を果たします。
結合組織の成分は、血管壁において局所的な機能要件に基づいて、さまざまな量と割合で存在します。コラーゲン繊維 (collagen fibers) は、基底膜下層や平滑筋層の間、また外膜 (adventitia) に見られます。弾性繊維 (elastic fibers) は、血管壁が圧力に対して拡張するために必要な弾力性を提供します。弾性繊維の主要な成分であるエラスチン (elastin) は、大動脈などの大動脈において、平滑筋層の間に規則的に配置された層を形成しています。異なる種類のプロテオグリカン (proteoglycans) やヒアルロン酸 (hyaluronate) などの基質成分の量や構成の違いは、異なる血管の壁の物理的および代謝的特性に寄与し、特にその透過性に影響を与えます。
微小血管より大きいすべての血管の壁には、多くの共通する成分があり、類似した構成をしています。血管の分岐はそのサイズを徐々に減少させ、血管壁の構成にも変化をもたらします。例えば、「細動脈 (small arteries)」から「細動脈 (arterioles)」への移行は明確ではありません。しかし、これらの大きな血管はすべて、3つの同心層、すなわち外膜、中膜、内膜 (tunics) を持っています(ラテン語のtunica は「コート」を意味します)。これについては図11-6と図11-7~図11-9で示されています。
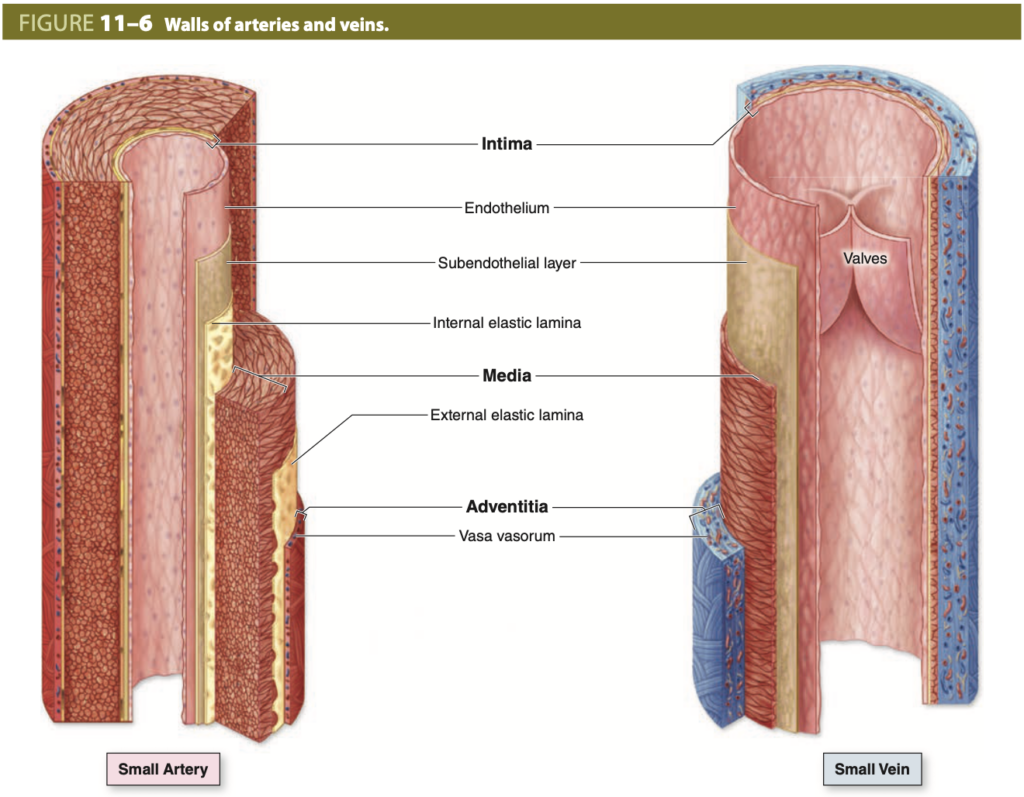
動脈と静脈の壁 (Walls of Arteries and Veins)
動脈と静脈の壁には、内膜 (intima)、中膜 (media)、外膜 (adventitia, または外層 externa) と呼ばれる3つの層(チュニック tunics)があります。これらは、心臓の内膜 (endocardium)、心筋 (myocardium)、および心外膜 (epicardium) におおよそ対応しています。動脈は、中膜が厚く、相対的に狭いルーメンを持ちます。一方、静脈はルーメンが広く、外膜が最も厚い層です。静脈の内膜はしばしばヒダを形成し、弁 (valves) を作ります。毛細血管 (capillaries) は内皮 (endothelium) のみで構成され、基底膜下層や他の層は存在しません。
- 最も内側の内膜 (tunica intima) は、内皮と疎性結合組織 (loose connective tissue) から成り、時には平滑筋繊維 (smooth muscle fibers) が含まれます(図11-7)。動脈では、内膜にはエラスチンから成る薄い層である内弾性板 (internal elastic lamina) が含まれており、これにより血液から血管壁への物質の拡散が容易になります。
- 中膜 (tunica media) は、主に螺旋状に配置された平滑筋細胞 (smooth muscle cells) の同心層で構成されています(図11-6および図11-7)。筋線維の間には、弾性繊維 (elastic fibers) や弾性板 (elastic lamellae)、細網繊維 (reticular fibers)、プロテオグリカン (proteoglycans) が含まれており、すべて平滑筋細胞によって生成されます。動脈では、中膜に外弾性板 (external elastic lamina) が存在し、これが外膜との間を隔てています。
- 最外層の外膜 (tunica adventitia) は、主にI型コラーゲン (type I collagen) と弾性繊維 (elastic fibers) から成る結合組織で構成されています(図11-7および図11-8)。外膜は、その血管が走行する臓器の間質 (stroma) と連続しています。
心臓の壁が冠動脈 (coronary vasculature) によって栄養や酸素を供給されるように、大きな血管にも栄養血管 (vasa vasorum, vessels of the vessel) があり、外膜や中膜の外側部分に細動脈 (arterioles)、毛細血管 (capillaries)、小静脈 (venules) が存在しています(図11-8)。大きな血管では壁が厚いため、ルーメン内の血液からの拡散だけでは栄養が十分に供給されません。ルーメン内の血液は、内膜にある細胞の必要を満たすだけです。大静脈 (large veins) では、酸素が少ない血液を運ぶため、通常、動脈よりも多くの栄養血管があります。
大きな血管の外膜には、無髄自律神経線維 (unmyelinated autonomic nerve fibers) のネットワークである血管運動神経 (vasomotor nerves) も含まれており、これが血管収縮物質ノルエピネフリン (norepinephrine) を放出します。動脈の方が静脈よりもこれらの神経支配が豊富です。
血管系 (Vasculature)
大きな血管および微小血管の血管は、頻繁に分岐し、異なる組織学的特徴や機能を持つ構造へと徐々に移行します。教育的な目的のために、血管はここで説明されているタイプとして分類され、表11-1にリストされています。
| 血管の種類 (Type of Artery) | 直径の範囲 (Outer Diameter) | 内膜 (Intima) | 中膜 (Media) | 外膜 (Adventitia) | 循環系における役割 (Roles in Circulatory System) |
|---|---|---|---|---|---|
| 弾性動脈 (Elastic arteries) | > 10 mm | 内皮 (Endothelium); 平滑筋を含む結合組織 (Connective tissue with smooth muscle) | 平滑筋と交互に配置された多数の弾性板 (Many elastic lamellae alternating with smooth muscle) | 中膜よりも薄い結合組織 (Connective tissue, thinner than media), 栄養血管あり (vasa vasorum present) | 心臓から血液を運び、弾性反動によって一定の圧力下で血流を維持 (Conduct blood from the heart; elastic recoil maintains steady pressure) |
| 筋性動脈 (Muscular arteries) | 10-1 mm | 内皮 (Endothelium); 平滑筋を含む結合組織 (Connective tissue with smooth muscle); 内弾性板が顕著 (Internal elastic lamina prominent) | 平滑筋層が多数存在し、弾性物質は少ない (Many smooth muscle layers, with less elastic material) | 中膜よりも薄い結合組織 (Connective tissue, thinner than media); 栄養血管がある場合も (vasa vasorum may be present) | 血液を全身に分配し、血圧と血流を維持 (Distribute blood to organs; maintain steady blood pressure and flow) |
| 小動脈 (Small arteries) | 1-0.1 mm | 内皮 (Endothelium); 平滑筋の少ない結合組織 (Connective tissue less smooth muscle) | 3-10層の平滑筋 (3-10 layers of smooth muscle) | 中膜よりも薄い結合組織 (Connective tissue, thinner than media); 栄養血管なし (no vasa vasorum) | 血液を細動脈に送り、血流を調整 (Distribute blood to arterioles; adjust blood flow) |
| 細動脈 (Arterioles) | 100-10 µm | 内皮 (Endothelium); 平滑筋や結合組織なし (No connective tissue or smooth muscle) | 1-3層の平滑筋 (1-3 layers of smooth muscle) | 非常に薄い結合組織層 (Very thin connective tissue layer) | 血流を抵抗・制御し、全身血圧の主な決定因子 (Resist and control blood flow; major determinant of systemic blood pressure) |
| 毛細血管 (Capillaries) | 10-4 µm | 内皮のみ (Endothelium only) | 少数の周皮細胞のみ (A few pericytes only) | なし (None) | 物質の交換 (Exchange of metabolites) |
| 小静脈 (Venules: 後毛細血管・収集・筋性) | 100-10 µm | 内皮 (Endothelium); 弁なし (No valves) | 周皮細胞と散在する平滑筋細胞 (Pericytes and scattered smooth muscle cells) | なし (None) | 毛細血管床からの排液 (Drain capillary beds); 白血球の血管外移動の場 (Site of leukocyte exit from vasculature) |
| 小静脈 (Small veins) | 1-0.1 mm | 内皮 (Endothelium); 散在する平滑筋線維を含む結合組織 (Connective tissue with scattered smooth muscle fibers) | 2-3層の緩い平滑筋 (2-3 loose layers of smooth muscle) | 中膜より厚い結合組織 (Connective tissue thicker than media) | 小静脈から血液を集める (Collect blood from venules) |
| 中型静脈 (Medium veins) | 1-10 mm | 内皮 (Endothelium); 弁あり (With valves) | 3-5層の明確な平滑筋 (3-5 distinct layers of smooth muscle) | 中膜より厚い (Thicker than media); 縦方向の平滑筋が存在することも (Longitudinal smooth muscle may be present) | 大静脈に血液を運ぶ (Carry blood to larger veins) |
| 大静脈 (Large veins) | > 10 mm | 内皮 (Endothelium); 平滑筋と結合組織を含む (Connective tissue, smooth muscle cells); 明瞭な弁あり (Prominent valves) | 5層以上の平滑筋と多くのコラーゲン (More than 5 layers of smooth muscle, with much collagen) | 最も厚い層 (Thickest layer), 縦方向の平滑筋が存在することも (Longitudinal smooth muscle bundles may be present) | 心臓に血液を戻す (Return blood to the heart) |
弾性動脈 (Elastic Arteries)
弾性動脈には、大動脈 (aorta)、肺動脈 (pulmonary artery)、およびそれらの大枝が含まれます。これらの大血管は「伝導動脈 (conducting arteries)」とも呼ばれ、主に血液を小さな動脈に運ぶ役割を果たします。図11-7aに示されているように、弾性動脈の最も顕著な特徴は、弾性板 (elastic lamellae) と平滑筋繊維の層が交互に配置された厚い中膜 (tunica media) です。成人の大動脈には約50の弾性板があり、高血圧の人ではさらに多くなります。
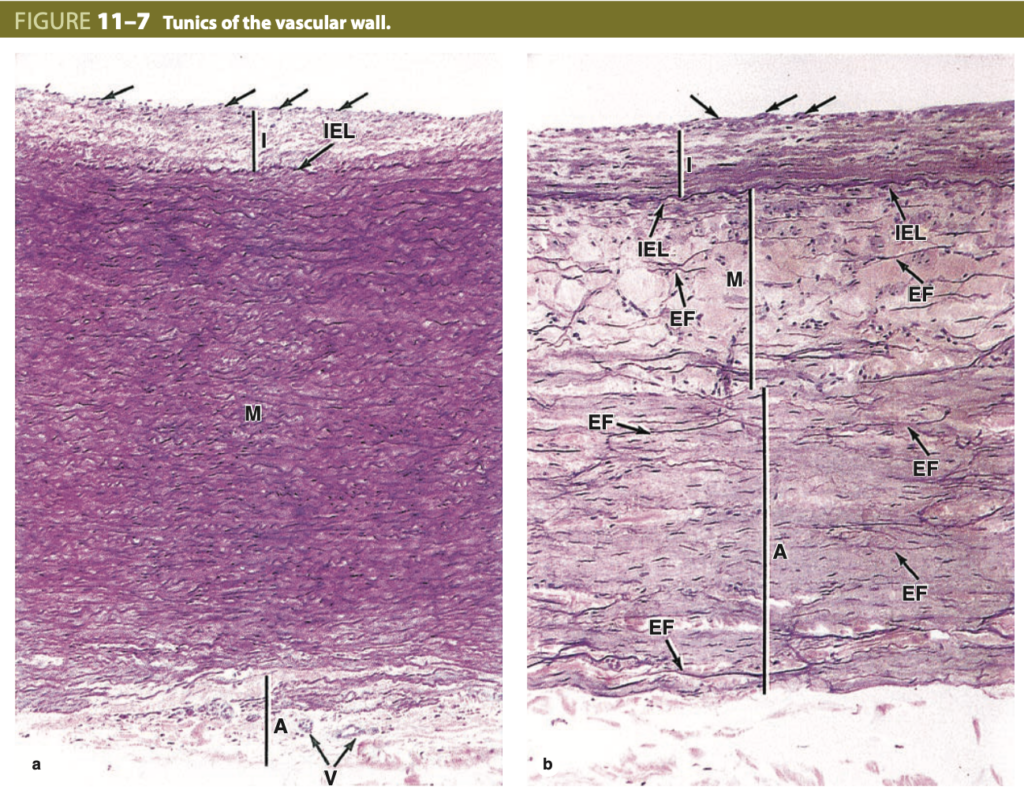
主要な動脈および静脈の3つの層の比較 (a) 大動脈 (Aorta), (b) 大静脈 (Vena cava)。内皮 (simple squamous endothelial cells, 矢印) は内膜 (intima, I) を覆い、動脈には基底膜下層の結合組織があり、内膜は内部弾性板 (internal elastic lamina, IEL) によって中膜 (media) と区切られています。この構造は、大静脈を除くほとんどの静脈には存在しません。中膜 (M) には、多くの弾性板 (elastic lamellae) と弾性繊維 (elastic fibers, EF) が平滑筋層と交互に配置されています。大動脈では、中膜が非常に厚く、弾性繊維が豊富です。外膜 (adventitia, A) にも弾性繊維が存在し、大静脈では外膜が相対的に厚いです。大動脈の外膜には、栄養血管 (vasa vasorum, V) が見られます。外膜の結合組織は、周囲の疎性結合組織と連続しています。
内膜 (tunica intima) は発達しており、基底膜下の結合組織に多くの平滑筋細胞が含まれ、血圧の低下や死後の血管収縮の結果として、断面図ではしばしば折りたたまれた様子が見られます (図11-8)。内膜と中膜の間には内弾性板 (internal elastic lamina) があり、中膜の弾性板よりもはっきりしています(図11-7aおよび図11-9)。外膜 (adventitia) は中膜よりも薄くなっています。
これらの動脈に含まれる多数の弾性板は、血流をより均一にするという重要な機能に寄与しています。心室が収縮 (systole) すると、血液は動脈を強制的に通り、エラスチン (elastin) が伸展し、壁はコラーゲンの制限内で拡張します。心室が弛緩 (diastole) すると心室の圧力は低下しますが、エラスチンは受動的に反発し、動脈圧を維持するのを助けます。大動脈弁および肺動脈弁は血液が心臓に逆流するのを防ぎ、反発により血流が心臓から離れて流れ続けます。動脈圧および血液の速度は、心臓からの距離が増すにつれて低下し、より一定になります。
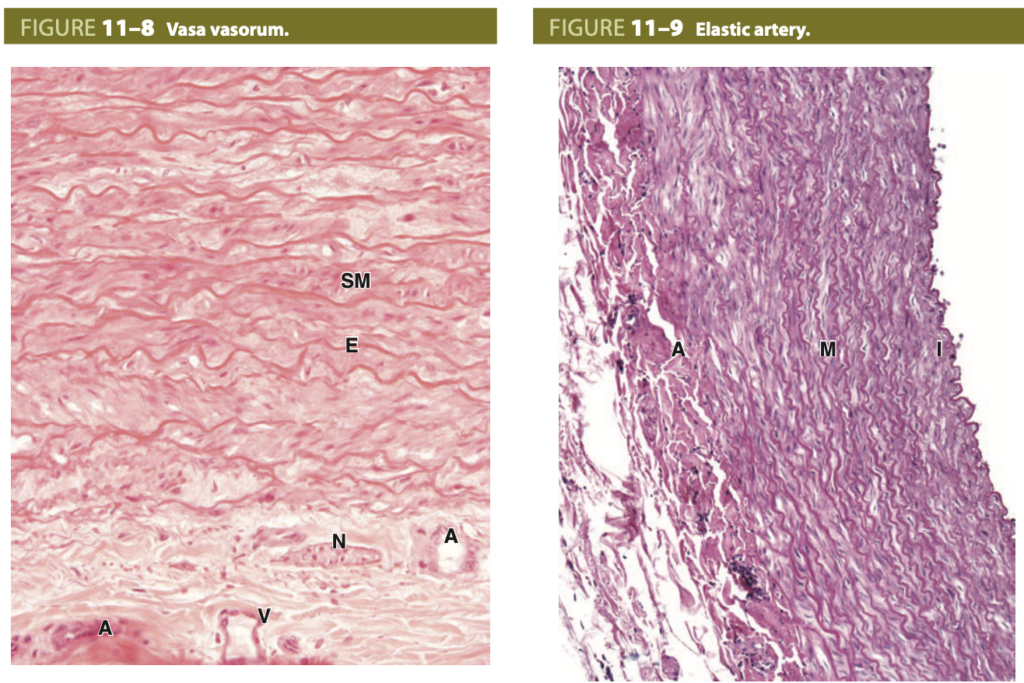
栄養血管 (Vasa Vasorum)
大きな動脈の外膜には、局所の細胞に酸素と栄養を供給する微小血管が含まれています。これらの血管(細動脈、毛細血管、小静脈)は、動脈の外膜に存在し、血管の壁の厚い部分に血液が届くのを助けます。図中の外膜の上方には、平滑筋線維 (SM) と弾性板 (E) が中膜に見られます。
弾性動脈 (Elastic Arteries)
最大の動脈は、かなりの量の弾性物質を含み、心臓の収縮時に拡張します。大きな弾性動脈の一部の横断切片では、主に多数の発達した弾性板 (elastic lamellae) から成る厚い中膜 (media) が見られます。心室収縮 (収縮期 systole) 時に動脈に脈動する血液の強い圧力が動脈壁を拡張させ、圧力を減少させ、心室弛緩 (拡張期 diastole) 中にも強い血流が続きます。空の大動脈の内膜 (intima) は通常、折りたたまれ、外膜 (adventitia) の密な不規則結合組織 (dense irregular connective tissue) は中膜よりも薄いです。
医学的応用 (Medical Application)
動脈硬化症 (atherosclerosis) は、弾性動脈および大きな筋性動脈の疾患であり、先進国における死亡原因の約半数に関与しています。動脈硬化症は、内皮細胞の損傷や機能不全によって引き起こされ、これにより低密度リポタンパク質 (LDL, low-density lipoproteins) が酸化され、内膜内で修飾されたLDLを除去するために単球やマクロファージが内膜に侵入し、付着します。脂肪を蓄えたマクロファージ(泡沫細胞 (foam cells))が蓄積し、修飾されたLDLとともに、初期の動脈硬化の病理的兆候である脂肪条 (fatty streaks) を形成します。病気が進行すると、これらは線維脂肪性プラーク (fibro-fatty plaques) またはアテローム (atheromas) に発展し、これには平滑筋細胞、コラーゲン繊維、リンパ球、壊死部位、および脂肪や細胞破片が含まれます。
動脈硬化症の発症に関与する要因としては、脂質異常症 (dyslipidemia)、高血糖 (hyperglycemia, 糖尿病)、高血圧 (hypertension)、および喫煙による毒素の存在が挙げられます。弾性動脈においては、アテロームが局所的な破壊を引き起こし、動脈瘤 (aneurysms) を形成して破裂する可能性があります。冠動脈のような筋性動脈では、アテロームが血流を閉塞し、虚血性心疾患 (ischemic heart disease) を引き起こすことがあります。
動脈感覚構造 (Arterial Sensory Structures)
頸動脈洞 (carotid sinuses) は、両側の内頸動脈 (internal carotid arteries) が弾性動脈 (elastic arteries) である総頸動脈 (common carotid arteries) から分岐する部分に存在するわずかな膨らみです。これらは動脈圧 (arterial blood pressure) を監視する重要な圧受容体 (baroreceptors) として機能します。この部分では、中膜 (tunica media) が薄くなり、血圧の上昇時により大きな伸展が可能となり、外膜 (adventitia) には多数の感覚神経終末が含まれ、これらは第IX脳神経である舌咽神経 (glossopharyngeal nerve) から派生しています。脳の血管運動中枢 (vasomotor centers) はこれらの求心性インパルスを処理し、血管の収縮を調整して血圧を正常に保ちます。機能的に類似した圧受容体は、大動脈弓 (aortic arch) にも存在し、第X脳神経である迷走神経 (vagus nerve) を介して血圧に関する信号を伝達します。
さらに複雑な組織学的構造を持つ化学受容体 (chemoreceptors) は、動脈血中の二酸化炭素 (CO₂) や酸素 (O₂) 濃度、pHを監視し、これらは頸動脈洞や大動脈弓の壁にある頸動脈小体 (carotid bodies) や大動脈小体 (aortic bodies) に存在します。これらの構造は、自律神経系の一部であり、傍神経節 (paraganglia) と呼ばれ、豊富な毛細血管網を持っています。毛細血管は、神経堤由来のグロムス細胞 (glomus cells) に密接に囲まれており、これらの細胞はドーパミン (dopamine)、アセチルコリン (acetylcholine) などの神経伝達物質を含む密集したコアを持つ小胞に満ちています。これらは小型の衛星細胞 (satellite cells) によって支持されています(図11-10)。グロムス細胞の膜にあるイオンチャネルは、低酸素症 (hypoxia)、高炭酸ガス血症 (hypercapnia)、またはアシドーシス (acidosis) など、動脈血中の刺激に反応して神経伝達物質の放出を促進します。これらの伝達物質が分泌されると、舌咽神経から分岐した感覚線維がシナプスを形成し、脳の中枢に信号を送り、心血管および呼吸系の調整が行われます。
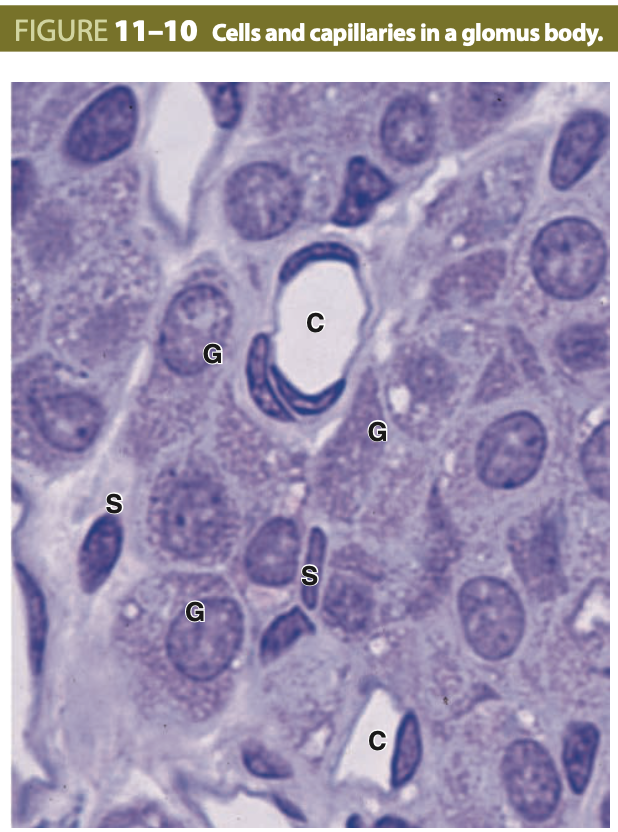
化学受容体として機能する組織 (Chemoreceptors)
特定の弾性動脈の壁にある特殊な組織は、血液の化学成分に関する情報を脳に提供する化学受容体 (chemoreceptors) として機能します。グロムス体 (glomus bodies) は、総頸動脈 (common carotid arteries) 付近に見られる2つの小さな神経節様構造(直径0.5〜5 mm)で、多くの大きな毛細血管 (capillaries, C) と、それらに囲まれたグロムス細胞 (glomus cells, G) の集まりが含まれています。グロムス細胞は、さまざまな神経伝達物質を含む小胞を満たしており、支持細胞 (satellite cells, S) によって包まれています。グロムス細胞は感覚神経線維とシナプス結合を形成し、血液中の二酸化炭素 (CO₂)、酸素 (O₂)、または水素イオン (H⁺) 濃度の顕著な変化を検出し、神経伝達物質を放出して感覚神経を活性化し、これらの情報を脳に伝達します。
筋性動脈 (Muscular Arteries)
筋性動脈は「分配動脈 (distributing arteries)」とも呼ばれ、臓器に血液を供給し、平滑筋が収縮または弛緩することで血圧を調整します。内膜 (tunica intima) には薄い基底膜下層があり、顕著な内弾性板 (internal elastic lamina) が存在します(図11-11)。中膜 (tunica media) には、40層以上の大きな平滑筋細胞が含まれており、弾性板の数は血管のサイズによって異なります。外弾性板 (external elastic lamina) は、大型の筋性動脈にのみ存在します。外膜 (adventitia) の結合組織には、リンパ毛細血管 (lymphatic capillaries)、栄養血管 (vasa vasorum)、および神経が含まれており、これらは中膜の外側部分にも侵入します。
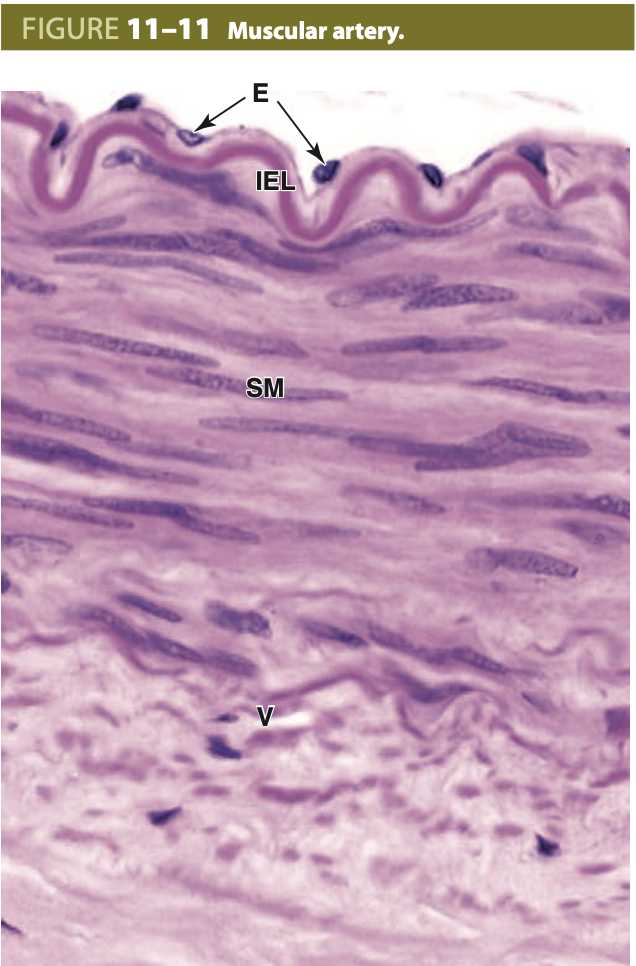
動脈の距離と壁の構造変化 (Changes in Artery Walls with Distance from the Heart)
心臓からの距離が離れるにつれて、動脈の壁には弾性繊維が相対的に減少し、平滑筋が増加します。名前がつけられるほど大きな動脈のほとんどは筋性動脈 (muscular arteries) タイプです。横断切片では、筋性(中型)動脈の内膜 (intima) がわずかに折りたたまれており、内皮細胞 (endothelial cells, E) と内部弾性板 (internal elastic lamina, IEL) の間に結合組織はほとんどありません。中膜 (media) の平滑筋層 (smooth muscle layers, SM) は、弾性繊維や弾性板よりも厚くなっています。外膜 (adventitia) には、栄養血管 (vasa vasorum) が見られます。
細動脈 (Arterioles)
筋性動脈は枝分かれを繰り返し、最終的に3〜4層の平滑筋細胞から成る小さな動脈になります。最も小さな動脈は細動脈 (arterioles) に分岐し、これらは1〜2層の平滑筋細胞しか持ちません。細動脈は臓器の微小血管系の始まりを示し、ここで血液と組織液の交換が行われます(図11-12および図11-13)。細動脈の直径は0.1mm未満で、ルーメンの幅は壁の厚さとほぼ同じです(図11-14)。基底膜下層は非常に薄く、弾性板は存在せず、中膜 (media) は円形に配置された平滑筋細胞で構成されています。小動脈および細動脈では、外膜は非常に薄く、目立ちません。
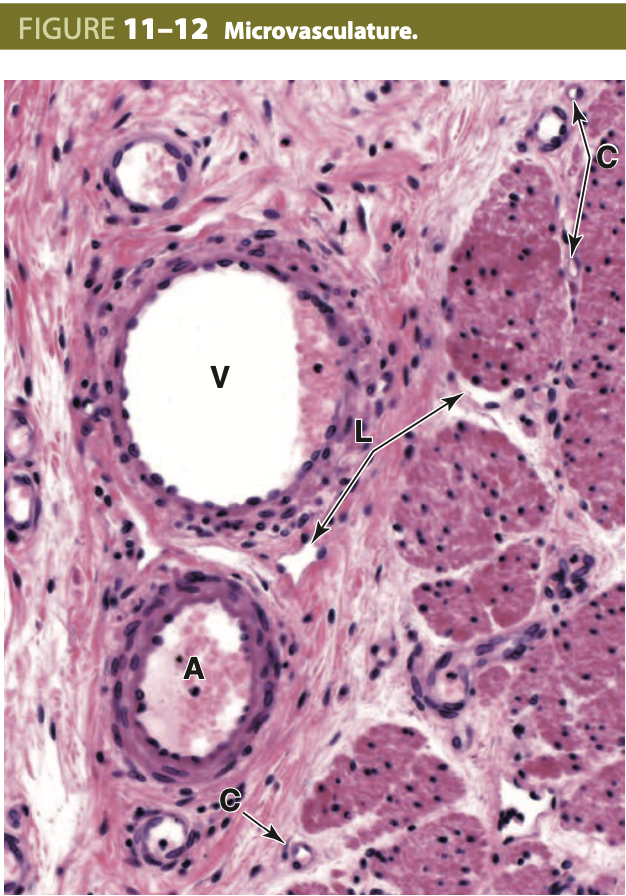
微小血管系の構成 (Components of Microvasculature)
細動脈 (arterioles)、毛細血管 (capillaries)、および小静脈 (venules) は、ほぼすべての臓器で微小血管系を構成し、血液と周囲の組織間で分子の交換が行われます。中膜や外膜がないこれらの血管は、直径がわずか4〜10μmであり、パラフィン切片では小さなルーメンに隣接する細胞核や、ルーメン内にある好酸性の赤血球によって認識されます。図5-20に記載されているように、毛細血管床で形成された間質液のすべてが小静脈に排出されるわけではなく、その余剰分はリンパ (lymph) として集められ、薄壁で不規則な形をしたリンパ管 (lymphatic vessels) に流れ込みます。
細動脈はほぼ常に分岐して毛細血管が臓器の実質細胞 (parenchymal cells) を取り囲む網状のネットワークを形成します。細動脈の末端では、平滑筋繊維が括約筋 (sphincters) として作用し、毛細血管への血液流を断続的に調整します(図11-13)。筋緊張が通常細動脈を部分的に閉じて血流を制限し、これによりこれらの血管が全身の血圧の主要な決定要因となります。
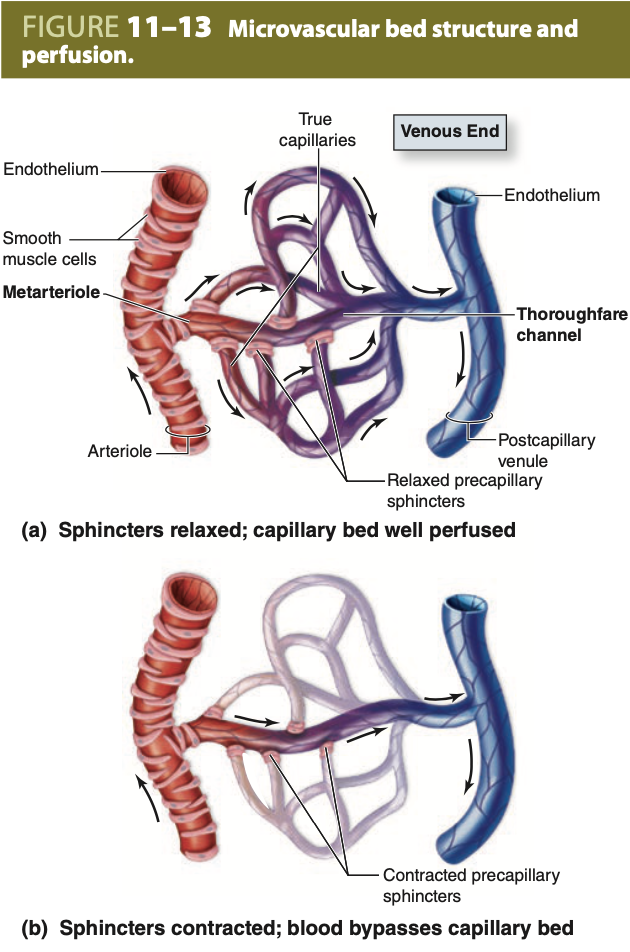
毛細血管床への血流の調節 (Regulation of Blood Flow to Capillary Beds)
毛細血管床に供給される細動脈は、通常、前毛細血管 (metarterioles) と呼ばれる小さな枝を形成し、ここでは平滑筋細胞が帯状に散在しており、前毛細血管括約筋 (precapillary sphincters) として作用します。前毛細血管の遠位部は、時折「通過路チャンネル (thoroughfare channel)」と呼ばれ、平滑筋細胞がなくなり、後毛細血管小静脈と合流します。前毛細血管と通過路チャンネルから分岐するのは、真の毛細血管 (true capillaries) であり、これらには平滑筋細胞は存在しませんが、周皮細胞 (pericytes) が存在することがあります。前毛細血管括約筋は、真の毛細血管への血流を調節します。 (a) すべての括約筋が弛緩し開いている、血流が良好な毛細血管床を示しています。 (b) 括約筋が収縮して血流がシャントされている毛細血管床を示しています。どの瞬間でも、ほとんどの括約筋は少なくとも部分的に閉じており、血液は脈動的に毛細血管床に流入し、栄養、老廃物、酸素 (O₂)、および二酸化炭素 (CO₂) の効率的な交換が内皮を通じて最大限に行われます。肺循環を除いて (図11-1)、血液はよく酸素化されて微小血管系に入り、酸素が少なくなって出ていきます。
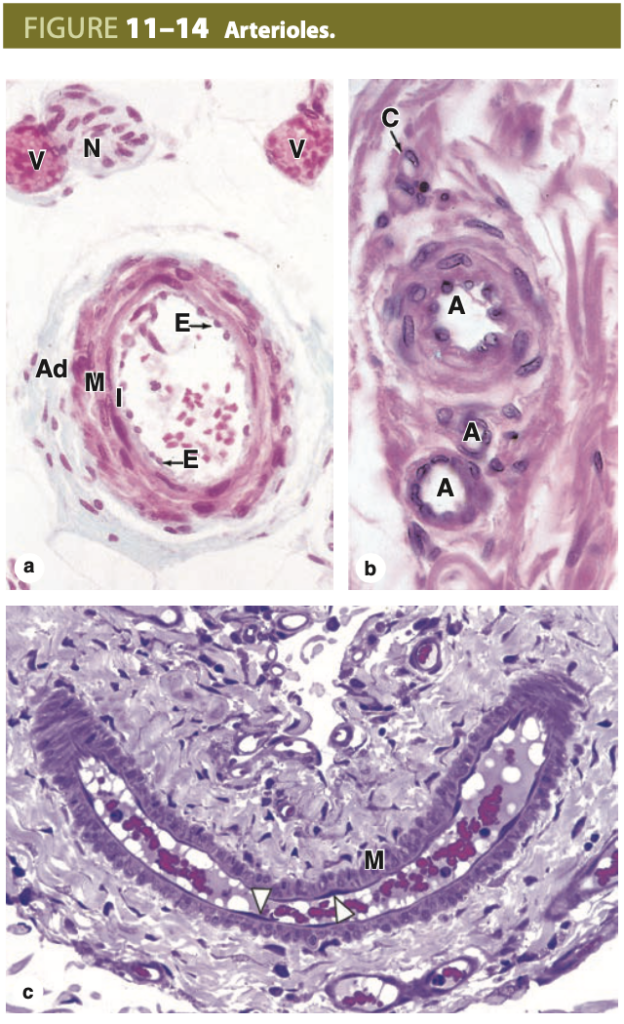
細動脈の構造 (Structure of Arterioles)
(a) 細動脈は、内皮細胞 (endothelial cells, E) のみから成る内膜 (intima, I) を持ち、細胞には丸い核が見られることがあります。中膜 (media, M) は1〜2層の平滑筋から成るチュニックであり、通常は目立たない薄い外膜 (adventitia, Ad) を持ちます。 (b) 様々なサイズの3つの細動脈 (A) と1つの毛細血管 (C) が示されています。 (c) 大きな腸間膜の細動脈を斜めおよび縦方向に切断した断面では、内皮細胞 (矢印頭) と横断的に切断された1〜2層の平滑筋細胞 (M) が明確に示されています。外膜 (adventitia) は隣接する結合組織と連続しています。
医学的応用 (Medical Application)
血圧は心拍出量 (cardiac output) と、主に細動脈の抵抗による全末梢血管抵抗 (total peripheral resistance) に依存します。高血圧 (hypertension) あるいは血圧の上昇は、腎臓や内分泌の問題によって二次的に生じる場合がありますが、より一般的には本態性高血圧 (essential hypertension) であり、細動脈の収縮を増加させるさまざまなメカニズムが関与しています。
特定の組織や臓器において、細動脈はさまざまな特殊機能に対応するために単純な経路から逸脱します(図11-15)。例えば、皮膚の体温調節 (thermoregulation) では、細動脈が毛細血管網を迂回して直接小静脈 (venules) に接続することができます。これらの動静脈短絡 (arteriovenous shunts) の中膜 (media) および外膜 (adventitia) は厚く、自律神経 (sympathetic and parasympathetic nerve fibers) が豊富に分布しています。自律神経は、短絡の血管収縮度を制御し、毛細血管床 (capillary beds) への血流を調節します。皮膚での高い毛細血管血流は体からの熱放散を促進し、逆に低い血流は熱を保持する機能を果たします。これらは、環境温度が高い場合や低い場合にそれぞれ重要な役割を果たします。
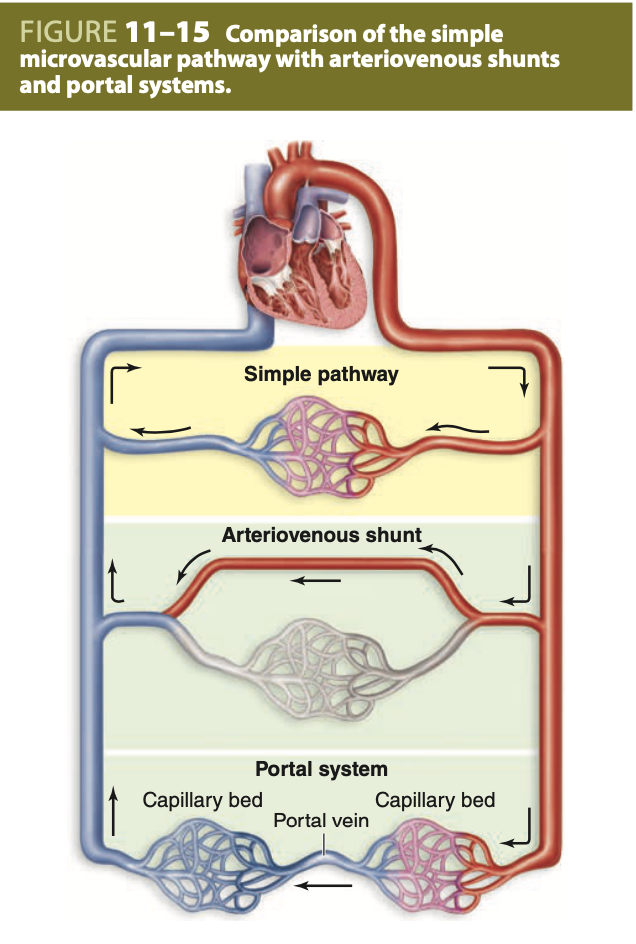
毛細血管床の代替経路 (Alternative Pathways in Capillary Beds)
毛細血管床のほとんどは細動脈によって供給され、小静脈に排出されますが、特定の臓器では代替経路が見られます。皮膚では、外的条件に応じて血流が動静脈吻合 (arteriovenous shunts, AV shunts) または吻合路 (anastomoses) によって調節され、毛細血管を一時的に迂回します。
静脈門脈系 (venous portal systems) では、1つの毛細血管床が静脈に排出され、その静脈が再び分岐して別の毛細血管床を形成します。この配置により、最初の毛細血管で血液に取り込まれた分子が2つ目の毛細血管床周囲の組織に速やかに高濃度で届けられることが可能となり、これは前下垂体 (anterior pituitary gland) および肝臓 (liver) で重要です。
もう一つの重要な微小血管経路は、静脈門脈系 (venous portal system) です(図11-15)。このシステムでは、血液が2つの連続した毛細血管床を通過し、それらは門脈 (portal vein) によって分離されています。この経路により、最初の毛細血管網で吸収されたホルモンや栄養素が、第2の毛細血管床周囲の細胞に効率的に届けられ、血液が心臓に戻る前に作用します。最も良い例は、肝門脈系 (hepatic portal system) と下垂体門脈系 (hypothalamic-hypophyseal portal system) であり、いずれも生理学的に重要です。
毛細血管床 (Capillary Beds)
毛細血管は、血液と周囲の組織との間の代謝交換を許可し、調整します。これらの最小の血管は常に毛細血管床 (capillary beds) と呼ばれるネットワークで機能し、そのサイズや全体の形状は供給される構造に対応します。毛細血管床の密度は、組織の代謝活動に関連しています。腎臓、肝臓、心筋、および骨格筋のような代謝率が高い組織には、豊富な毛細血管が存在します。これに対して、平滑筋や密な結合組織など代謝率が低い組織には、毛細血管が少なくなります。f
毛細血管床は、終末細動脈 (terminal arterioles) の枝である前毛細血管 (metarterioles) によって優先的に供給され、これらは通路チャンネル (thoroughfare channels) と連続しており、後毛細血管小静脈 (postcapillary venules) と接続します(図11-13)。毛細血管は、前毛細血管から分岐し、散在する平滑筋細胞に囲まれており、通路チャンネルへ合流します。通路チャンネルは筋肉を欠いています。前毛細血管の平滑筋細胞は、前毛細血管括約筋 (precapillary sphincters) として作用し、毛細血管への血液流入を制御します。これらの括約筋は周期的に収縮と弛緩を繰り返し、5~10分間隔で血液が毛細血管を脈動的に通過するようになります。括約筋が閉じているとき、血液は前毛細血管および通路チャンネルを通じて直接後毛細血管小静脈に流れ込みます。
毛細血管は、基底膜 (basement membrane) に囲まれた単層の内皮細胞 (endothelial cells) で構成され、管状に巻かれています(図11-16)。毛細血管の平均直径は4~10μmで、血球が1個ずつしか通過できないようになっており、それぞれの長さは通常50μm未満です。これらの非常に小さな血管は、体の血管系の90%以上を占め、その総長は10万km以上、総表面積は約5000平方メートルに及びます。括約筋の周期的な開閉により、大部分の毛細血管はほとんど空の状態であり、成人の総血液量の約5%(約300mL)がこれらの構造を通過しています。毛細血管の薄い壁、広範な表面積、および遅く断続的な血流は、血液と組織の間の水や溶質の交換を最適化します。
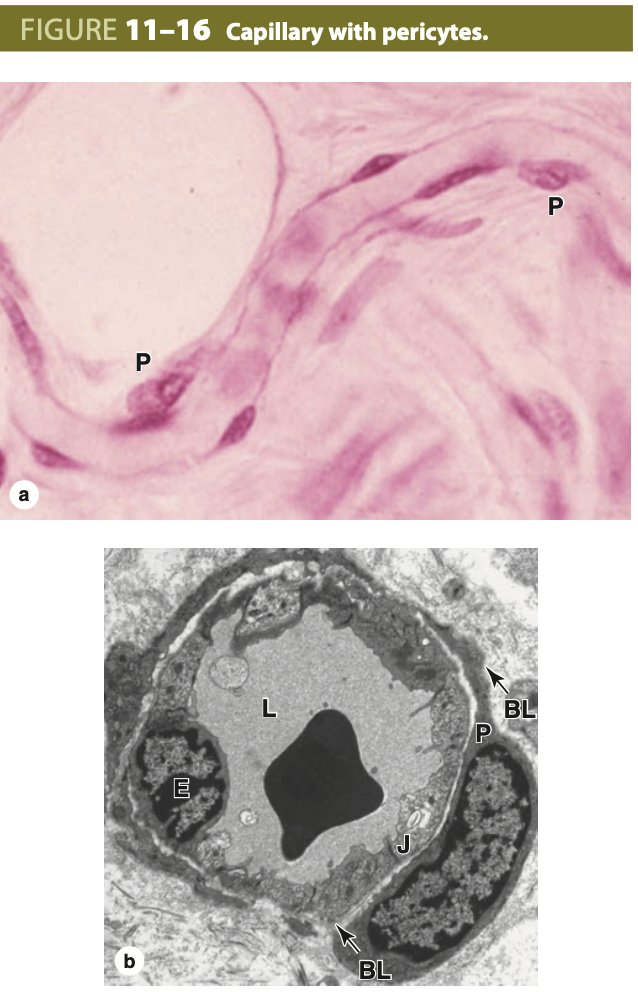
毛細血管 (Capillaries) は内皮 (endothelium) で形成されたチューブであり、血液と組織液との間で分子の交換が行われます。
(a) 毛細血管は通常、周皮細胞 (pericytes, P) と呼ばれる血管周囲の収縮細胞に関連しています。これらの細胞にはさまざまな機能があります。より扁平な核は内皮細胞 (endothelial cells) に属しています。(X400; H&E のメセンテリー標本) (b) 横断的に切断された毛細血管の透過型電子顕微鏡像 (TEM) では、1つの薄い毛細血管内皮細胞 (E) の核が示されています。内皮細胞は毛細血管のルーメン (L) を形成し、基底膜 (basal lamina, BL) で覆われ、接合複合体 (junctional complexes, J) によってしっかりと結合されています。1つの周皮細胞 (pericyte, P) が見られ、独自の基底膜 (BL) に囲まれ、内皮細胞を囲む細胞質の伸長を持っています。(X13,000)
前述の内皮の性質に加え、毛細血管の細胞には単純拡散からトランスサイトーシスまで、分子の転送に特化した多くの機能があります。細胞の平均厚さはわずか0.25μmで、細胞核は非常に小さな管状構造に適応するために独特に曲がっていることがよくあります(図11-10)。細胞質にはミトコンドリアや他の細胞小器官が含まれており、多くの膜小胞も存在します。基底膜とともに、細胞間接合複合体が管状構造を維持し、変動する数のタイトジャンクションが毛細血管の透過性に重要な役割を果たしています。
臓器によって、毛細血管の構造には大きな変動があり、これによりさまざまなレベルの代謝交換が可能となります。毛細血管は、内皮細胞と基底膜の連続性に基づいて、一般的に3つの組織学的タイプに分類されます(図11-17から図11-20まで)。
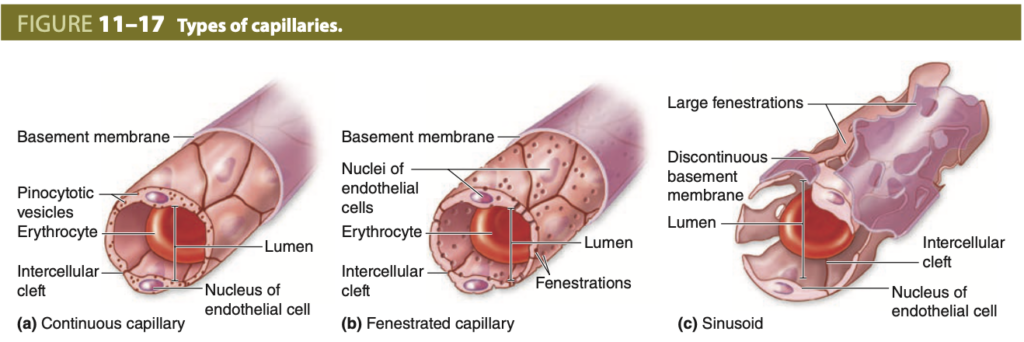
毛細血管の3つのタイプ (Three Types of Capillaries)
動脈から小静脈へ至る間の血管は、3つのタイプに分類されます。
(a) 連続性毛細血管 (Continuous capillaries) は、最も一般的なタイプであり、すべての内皮細胞の間の細胞間裂を閉じるためにタイトな閉鎖接合 (occluding junctions) を持ち、流体の漏出を最小限に抑えます。内皮を横断して交換されるすべての分子は、拡散やトランスサイトーシス (transcytosis) を介して細胞を通過する必要があります。
(b) 有窓性毛細血管 (Fenestrated capillaries) は、タイトな接合を持っていますが、内皮細胞内にある小さな孔 (フェネストレーション fenestrations) によって、内皮を通じたより多くの交換が可能です。これらの毛細血管タイプでは、基底膜 (basement membrane) は連続しています。有窓性毛細血管は、血液との分子交換が重要な内分泌器官、腸壁、脈絡叢 (choroid plexus) などに見られます。
(c) 洞様毛細血管 (Sinusoids, または不連続性毛細血管 discontinuous capillaries) は、他のタイプよりも広い直径を持ち、内皮細胞間に不連続性があり、細胞を通じた大きなフェネストレーションや部分的に不連続な基底膜を持ちます。洞様毛細血管は、骨髄 (bone marrow)、肝臓 (liver)、脾臓 (spleen) などの臓器で見られ、血液と組織の間でのマクロ分子や細胞の交換が容易に行われます。
- 連続性毛細血管 (Continuous capillaries)(図11-17a)は、わずかに重なり合う内皮細胞の間に発達した閉塞性接合 (occluding junctions) が多く存在し、内皮の連続性を提供し、細胞を通じた代謝交換をよく制御します。これは最も一般的な毛細血管タイプであり、筋肉、結合組織、肺、外分泌腺、神経組織で見られます。超微細構造の研究では、マクロ分子のトランスサイトーシスを示す多くの小胞が観察されています。
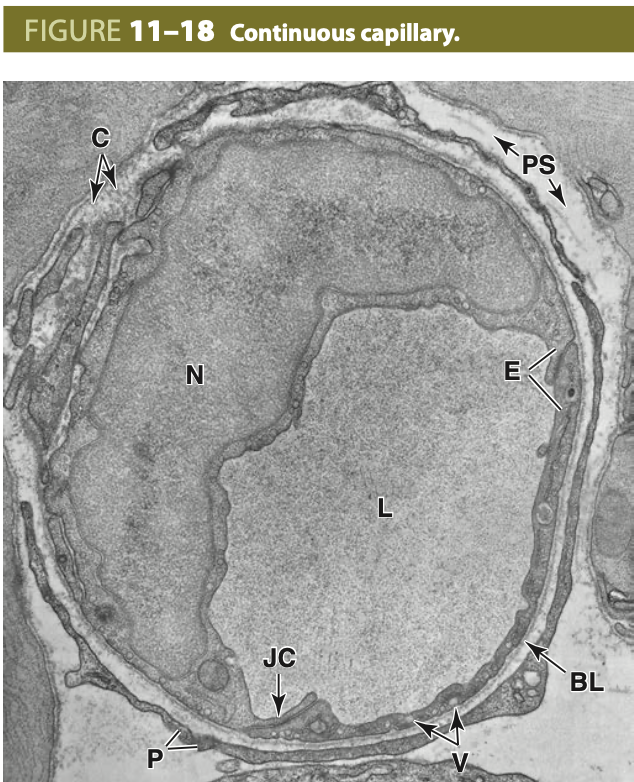
連続性毛細血管の構造 (Structure of Continuous Capillaries)
連続性毛細血管は、キャピラリーのルーメン (L) に出入りする分子を厳密に制御します。この電子顕微鏡像では、横断切片の連続性毛細血管が示されています。内皮細胞の核 (N) が目立ち、内皮細胞間の重なり部分にある接合複合体 (JC) でタイトな接合が豊富に存在しています。多くのトランスサイトーシス小胞 (V) が確認されます。連続性毛細血管の内皮を横断するすべての物質は、通常、拡散やトランスサイトーシスを通じて細胞内を通過しなければなりません。毛細血管の周囲には、基底膜 (BL) と周皮細胞 (P) の細胞質の薄い伸長があります。周囲の組織間隙 (PS) にはコラーゲン繊維 (C) や他の細胞外物質が見られます。(X10,000)
- 有窓性毛細血管 (Fenestrated capillaries)(図11-17b)は、内皮を通じたより広範な分子交換を可能にする篩状 (sieve-like) 構造を持っています。内皮細胞には多数の小さな円形の開口部、すなわちフェネストレーション (fenestrations)(ラテン語で「開口」を意味する)があります。その直径は約80nmです。いくつかのフェネストレーションは、プロテオグリカン (proteoglycans) の非常に薄い膜で覆われており、他のものはトランスサイトーシス中に一時的に両側を貫通する膜の陥入である場合があります。基底膜は連続しており、フェネストレーションを覆っています。有窓性毛細血管は、腎臓、腸、脈絡叢、内分泌腺など、組織と血液の間で物質の急速な交換が行われる臓器に見られます。
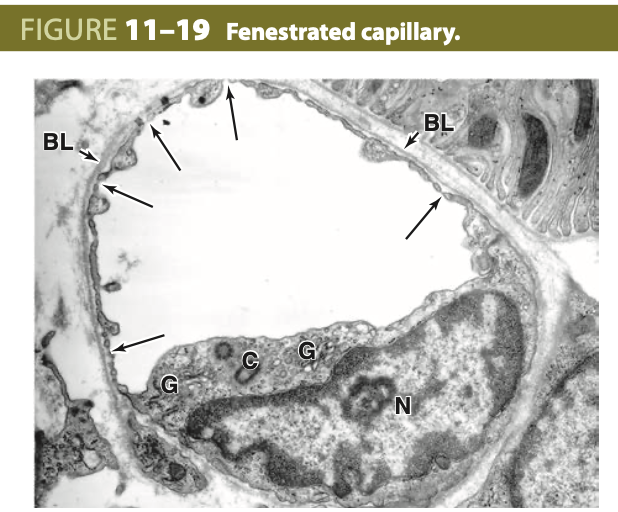
有窓性毛細血管の特殊化 (Specialization of Fenestrated Capillaries)
有窓性毛細血管は、内分泌腺などの臓器での分子の取り込みや腎臓の濾過システムでの分子の排出に特化しています。腎臓の尿細管周囲領域にある有窓性毛細血管の横断切片のTEMでは、膜で閉じられた典型的なフェネストレーションが多数見られます。内皮細胞を囲む連続した基底膜 (BL) も示されています。この細胞内にはゴルジ装置 (G)、核 (N)、中心体 (C) も見られます。有窓性毛細血管は、連続性毛細血管よりも分子の交換がより自由であり、腸壁、腎臓、内分泌腺に見られます。(X10,000) (ニューヨーク大学医科大学院、ヨハネス・ローディン博士の許可を得て使用)
- 不連続性毛細血管 (Discontinuous capillaries)、一般には洞様毛細血管 (sinusoids)(図11-17c)は、マクロ分子の最大限の交換や、細胞が組織と血液の間を容易に移動できるようにします。ここでは、内皮は大きな穴を持ち、膜で覆われておらず、細胞間に不規則な隙間を持つ不連続な層を形成しています。他の毛細血管とは異なり、洞様毛細血管の基底膜も高度に不連続であり、直径はしばしば30〜40μmと大きく、血流を遅くします。このタイプの洞様毛細血管は、肝臓、脾臓、一部の内分泌臓器、骨髄で見られます(図11-20)。
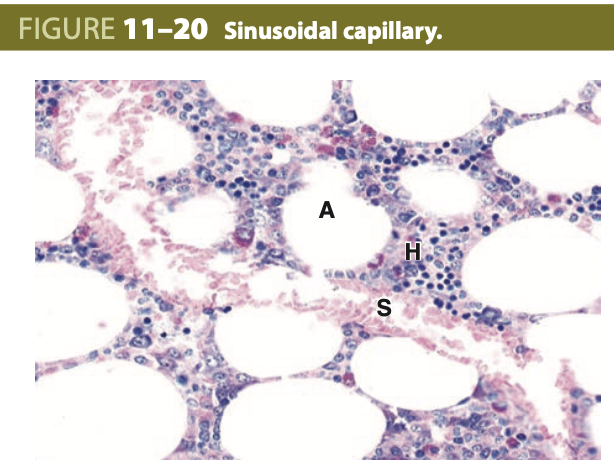
洞様毛細血管(Sinusoidal Capillaries または Sinusoids)
一般に、洞様毛細血管はほとんどの毛細血管よりも直径がはるかに大きく、血液と周囲の組織との間での最大限の分子交換や、血液細胞が内皮を通過するための容易な移動に特化しています。ここで示されている洞様毛細血管 (S) は骨髄 (bone marrow) にあり、脂肪細胞 (adipocytes, A) と造血細胞 (hematopoietic cells, H) の集まりに囲まれています。内皮細胞は非常に薄く、小さい毛細血管に比べて細胞核が見つけにくくなっています。電子顕微鏡で観察すると、洞様毛細血管には細胞間の大きな不連続性と基底膜を通じた大きなフェネストレーションが見られます。(X200; H&E)
連続性毛細血管および後毛細血管小静脈 (postcapillary venules) のいくつかの場所には、内皮層を部分的に取り囲む長い細胞質突起を持つ周皮細胞 (pericytes) という間葉系細胞が存在します(ギリシャ語で “peri” は「周囲」、”kytos” は「細胞」)。周皮細胞は多くの細胞外マトリックス (ECM, extracellular matrix) 成分を分泌し、自身の基底膜を形成して、内皮細胞の基底膜と融合します(図11-16)。周皮細胞には、ミオシン (myosin)、アクチン (actin)、およびトロポミオシン (tropomyosin) から成るよく発達した細胞骨格ネットワークがあり、これにより周皮細胞は毛細血管を収縮または拡張させ、いくつかの臓器で血流を調節します。中枢神経系 (CNS) では、周皮細胞は血液脳関門 (blood-brain barrier) の維持に重要な役割を果たします。傷害を受けた後、周皮細胞は増殖し、新しい血管の形成時に平滑筋細胞や他の細胞に分化して、微小血管系が再構築されます。多くの臓器では、周皮細胞の集団には、他の組織の再生に重要な間葉系幹細胞 (mesenchymal stem cells) も含まれています。
医学的応用 (Medical Application)
糖尿病 (diabetes) によって引き起こされる高血糖 (hyperglycemia) は、通常、糖尿病性微小血管障害 (diabetic microangiopathy) を引き起こし、これは毛細血管の基底膜の拡散性肥厚を伴い、これにより特に腎臓 (kidneys)、網膜 (retina)、骨格筋 (skeletal muscle)、および皮膚 (skin) において、代謝交換が減少します。
小静脈 (Venules)
毛細血管から小静脈への移行は徐々に進行します。後毛細血管小静脈 (postcapillary venules)(図11-21a)は、周皮細胞を含む毛細血管に類似していますが、直径が15~20µmと大きくなっています。血液に関する第12章で説明されているように、後毛細血管小静脈は、白血球 (white blood cells) が内皮に付着し、感染や組織損傷の部位で循環から離脱する主な場所です。後毛細血管小静脈は、より大きな収集小静脈 (collecting venules) に合流し、そこではより明確な収縮性細胞が見られます。小静脈のサイズが大きくなるにつれて、2~3層の平滑筋層を持つ明確な中膜 (tunica media) が小静脈を囲むようになり、これらは筋性小静脈 (muscular venules) と呼ばれます。すべての小静脈の特徴は、全体的に薄い壁に対してルーメンが非常に大きいことです(図11-21)。
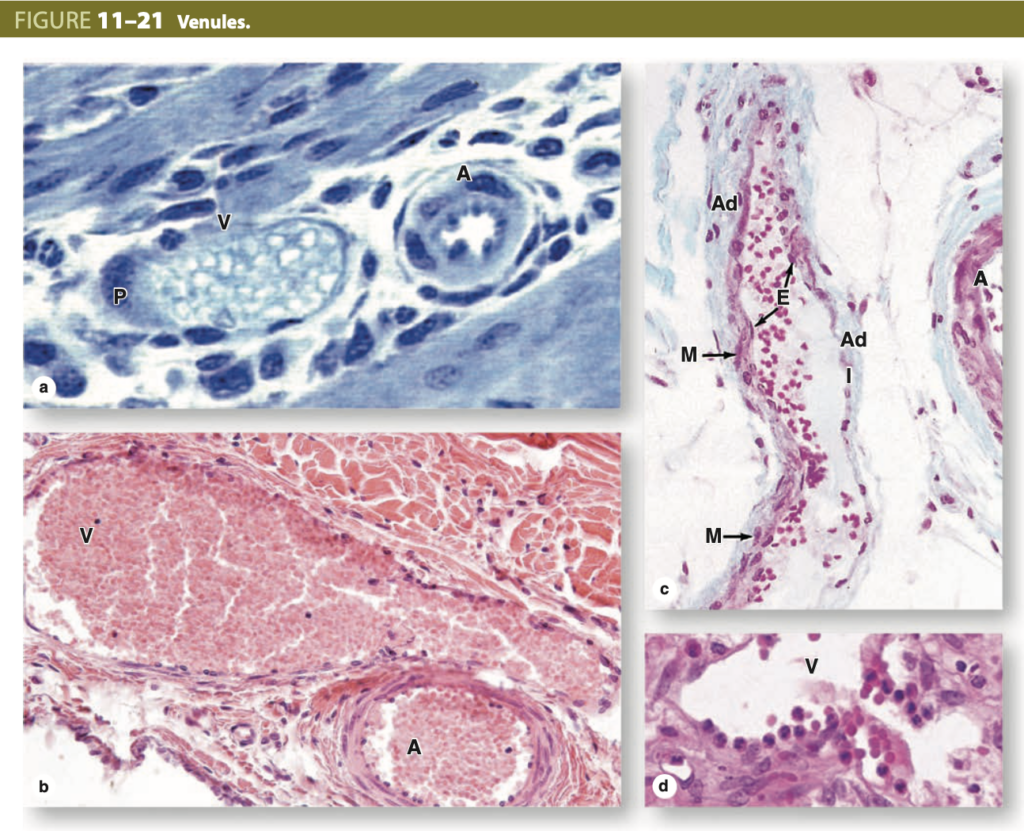
小静脈から静脈への移行 (Transition from Venules to Veins)
一連の徐々に大きく、より組織化された小静脈が毛細血管と静脈の間に存在します。
(a) 細動脈 (A) に比べて、後毛細血管小静脈 (postcapillary venules, V) は大きなルーメンを持ち、単純な内皮細胞 (endothelial cells) からなる内膜を持ち、時折周皮細胞 (pericytes, P) が見られます。(X400; Toluidine blue [TB])
(b) より大きな収集小静脈 (collecting venules, V) は、細動脈 (A) に比べて直径がはるかに大きいですが、壁は非常に薄く、内皮とより多くの周皮細胞または平滑筋細胞から成ります。(X200; H&E)
(c) 縦方向に切断された筋性小静脈 (muscular venule) では、明確な中膜が見られ、一部の領域では3層にまでなる平滑筋 (smooth muscle, M) 層を持ち、非常に薄い内膜 (intima, I) が内皮細胞 (E) で構成されています。部分的に切断された細動脈 (A) は、小静脈よりも厚い壁を持ちます。(X200; Masson trichrome) 白血球に関する第12章で述べたように、後毛細血管小静脈は、これらの細胞が循環から離れ、炎症や感染がある組織で機能する場所です。
(d) 感染した小腸から採取した後毛細血管小静脈 (V) では、いくつかの白血球 (leukocytes) が内膜に付着し、そこを横断している様子が見られます。(X200; H&E)
静脈 (Veins)
静脈は、全身の微小血管系から心臓に血液を戻します。静脈に入る血液は非常に低圧であり、主に中膜 (media) の平滑筋繊維の収縮や、周囲の骨格筋や他の臓器からの外部圧迫によって心臓に向かって移動します。ほとんどの静脈は小静脈 (small veins) または中型静脈 (medium veins) に分類され、直径は10mm以下です(表11-1)。これらの静脈は通常、対応する筋性動脈と並行して近くに位置しています。内膜 (tunica intima) は通常薄く、中膜 (media) には細い平滑筋細胞の束が網状繊維 (reticular fibers) とデリケートな弾性繊維 (elastic fibers) と混ざり合っており、膠原性外膜層 (collagenous adventitia layer) は厚く、よく発達しています。
大静脈 (large veins) は、心臓近くの弾性動脈と対になっている大きな静脈幹です(図11-7b)。これらの静脈は発達した内膜 (intima) 層を持っていますが、中膜は比較的薄く、平滑筋と結合組織が交互に配置されています。外膜 (tunica adventitia) は中膜よりも厚く、しばしば平滑筋の縦方向の束が含まれています。中膜と外膜の両方には弾性繊維が含まれ、動脈のような内弾性板が存在することもあります。
大静脈および中型静脈の重要な特徴は、静脈のルーメンを横切って突出する弁 (valves) です。これらの弁は、弾性繊維が豊富な内膜の薄い二重のひだで構成されており、両側が内皮に覆われています(図11-22および図11-23)。弁は特に脚部の静脈に多数存在し、静脈血を心臓に向かわせる役割を果たします。
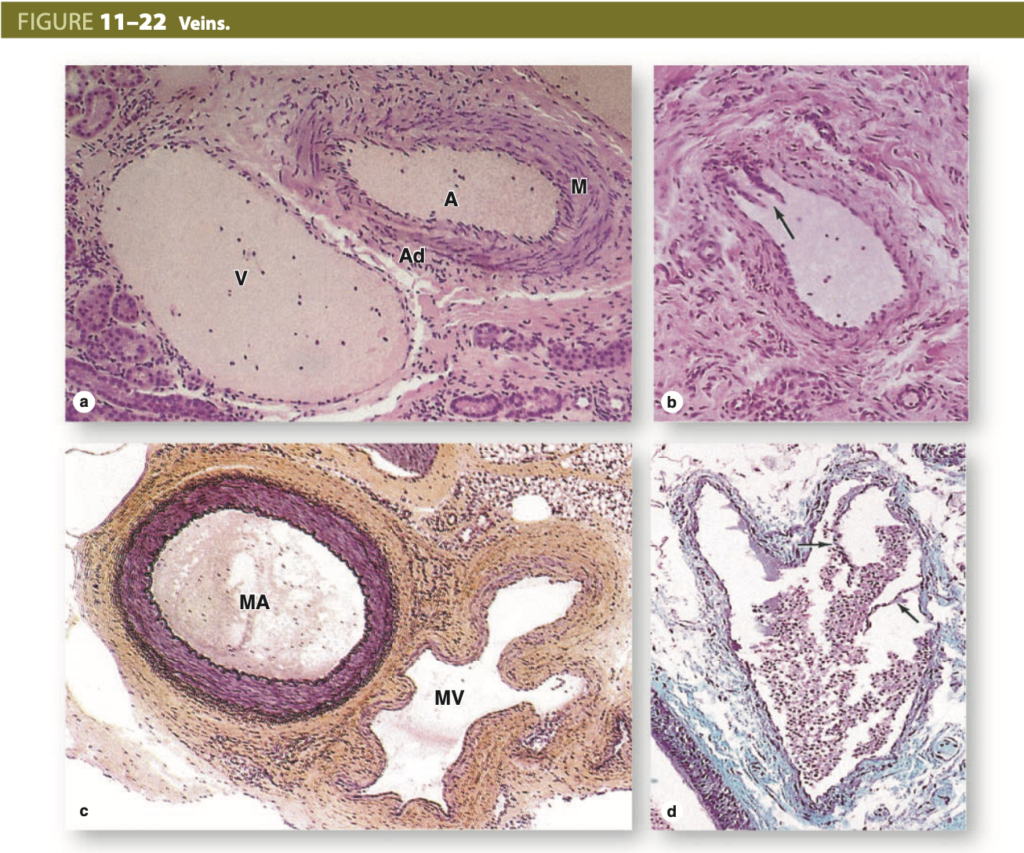
静脈の構造 (Structure of Veins)
静脈は通常、動脈と並んで走行し、サイズとチュニックの発達度に基づいて小静脈、中型静脈、大静脈に分類されます。
(a) 小静脈 (small vein, V) の顕微鏡像では、ルーメンが比較的大きく、厚い中膜 (media, M) と外膜 (adventitia, Ad) を持つ小さな筋性動脈 (muscular artery, A) が見られます。小静脈の壁は非常に薄く、2〜3層の平滑筋しか含まれていません。(X200; H&E)
(b) 小静脈 (small vein) の斜断面で、矢印で示された弁 (valve) が見られます。弁は、ルーメンに向かって突出する内膜の薄いヒダであり、血液の逆流を防ぐ役割を果たします。(X200; Aldehyde fuchsin & van Gieson)
(c) 中型静脈 (medium vein, MV) の顕微鏡像では、壁がやや厚くなっていますが、隣接する筋性動脈 (muscular artery, MA) に比べてまだそれほど顕著ではありません。中膜と外膜はより発達していますが、壁は相対的に大きなルーメンの周囲でしばしば折りたたまれています。(X100; Aldehyde fuchsin & van Gieson)
(d) 中型静脈 (medium vein) の顕微鏡像には血液が含まれており、弁のヒダ (valve folds, 矢印) が見られます。(X200; Masson trichrome)
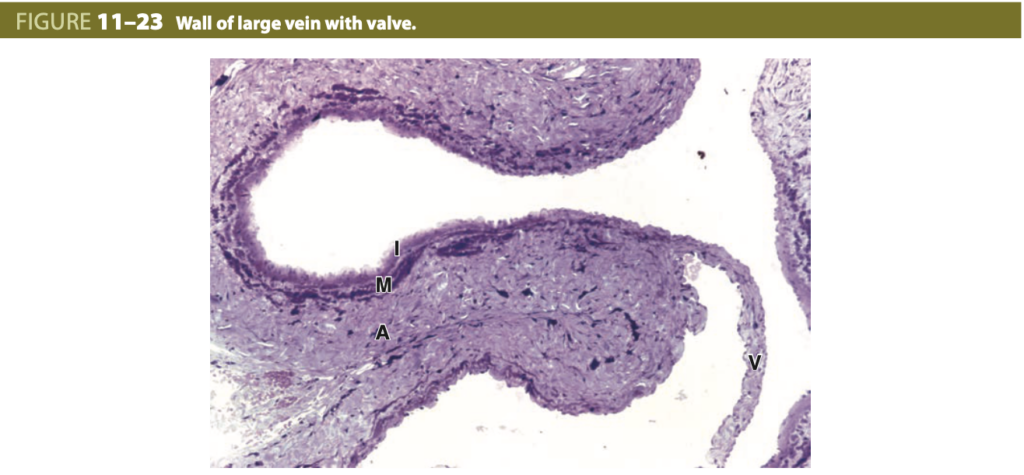
大静脈 (Large Veins)
大静脈には筋性の中膜 (media, M) があり、外膜 (adventitia, A) の密な不規則結合組織と比較して非常に薄くなっています。この壁はしばしば折りたたまれ、内膜 (intima, I) がルーメンに向かって突出し、内皮で覆われた基底膜下の結合組織で構成される弁 (valve, V) を形成しています。(X100; PT)
医学的応用 (Medical Application)
後毛細血管小静脈の内皮細胞間の接合部は、微小血管系で最も緩いものです。これにより、炎症 (inflammation) の際に白血球の経内皮移行 (transendothelial migration) が容易になり、炎症反応中にここでの液体の損失が特徴的であり、組織浮腫 (tissue edema) を引き起こします。
リンパ系血管 (Lymphatic Vascular System)
血管系に加えて、体内には非常に薄い壁を持つリンパ毛細血管 (lymphatic capillaries) というチャンネルのシステムがあり、組織間の余分な間質液 (interstitial fluid) をリンパ (lymph) として集め、血液に戻します。リンパは、間質液と同様に、淡い染色を示すたんぱく質が豊富ですが、通常は赤血球 (red blood cells) を含みません。ただし、リンパ球 (lymphocytes) や他の白血球 (white blood cells) が含まれていることがあります(図11-24a)。骨髄 (bone marrow) や中枢神経系 (CNS) の大部分などの例外を除いて、血液の微小血管があるほとんどの組織にはリンパ毛細血管(リンパ管とも呼ばれる)が存在します。
リンパ毛細血管は、非常に薄い内皮細胞 (endothelial cells) からなる管として局所的に始まり、これらはタイトジャンクション (tight junctions) を持たず、不連続な基底膜 (basal lamina) の上に位置します。コラーゲン (collagen) から成る細かい固定フィラメントが基底膜から周囲の結合組織に伸びており、これにより血管の崩壊を防ぎます。間質液は、内皮細胞間を通って、またはトランスサイトーシス (transcytosis) によってリンパ毛細血管に入ります。隣接する内皮細胞の特定の領域にはヘミデスモソーム (hemidesmosomes) が基底膜と接続しておらず、ルーメン (lumen) に向かって伸びてバルブの小葉を形成し、液体の流入を促進し、リンパの逆流をほとんど防ぎます(図11-24b)。
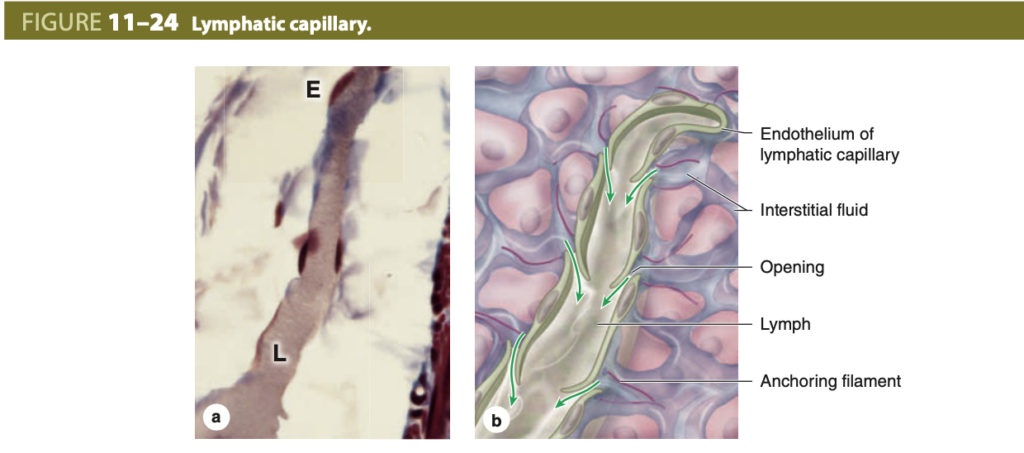
リンパ毛細血管 (Lymphatic Capillaries) は、微小血管系 (microvasculature) から押し出された血漿が、浸透圧の作用で再び血液に戻らなかった際に生成される間質液 (interstitial fluid) を排出します。
(a) 顕微鏡写真には、リンパ液 (lymph, L) で満たされたリンパ毛細血管が示されています。リンパ管 (lymphatics) は盲端を持つ血管で、非常に薄い内皮細胞 (endothelial cells, E) の壁で構成されており、直径は非常に変動します (10-50μm)。リンパはタンパク質や他の物質が豊富で、しばしば周囲の基質よりもややよく染色されます。(X200; Mallory trichrome)
(b) 図には、リンパ管に関するさらに多くの詳細が示されています。内皮細胞間の開口部が含まれており、これらの開口部はエラスチン (elastin) を含む固定フィラメントで支えられ、内皮細胞の伸長部分で覆われています。間質液は主にこれらの開口部を通ってリンパ管に入り、内皮細胞のヒダがリンパ液の組織への逆流を防ぎます。リンパ管の内皮細胞は、血液毛細血管の細胞よりも大きいのが一般的です。
リンパ毛細血管は、結合組織と平滑筋 (smooth muscle) の量が増加する薄い壁を持つより大きなリンパ管 (lymphatic vessels) に収束し、これらは明確な外層のチュニック (tunics) を形成することはありません(図11-25)。静脈と同様に、リンパ管には完全な内膜ヒダで構成されたバルブがあり、リンパの流れを一方向に保つ役割を果たします。これらの大きなリンパ管の経路には、リンパが免疫系の細胞によって処理されるリンパ節 (lymph nodes) が介在しています(第14章で詳述)。組織学的断面では、リンパ管はリンパで膨張していることがよくあります。静脈と同様に、リンパの循環は、周囲の骨格筋 (skeletal muscle) の収縮などの外部の力によって助けられ、バルブがリンパの流れを一方向に保ちます。
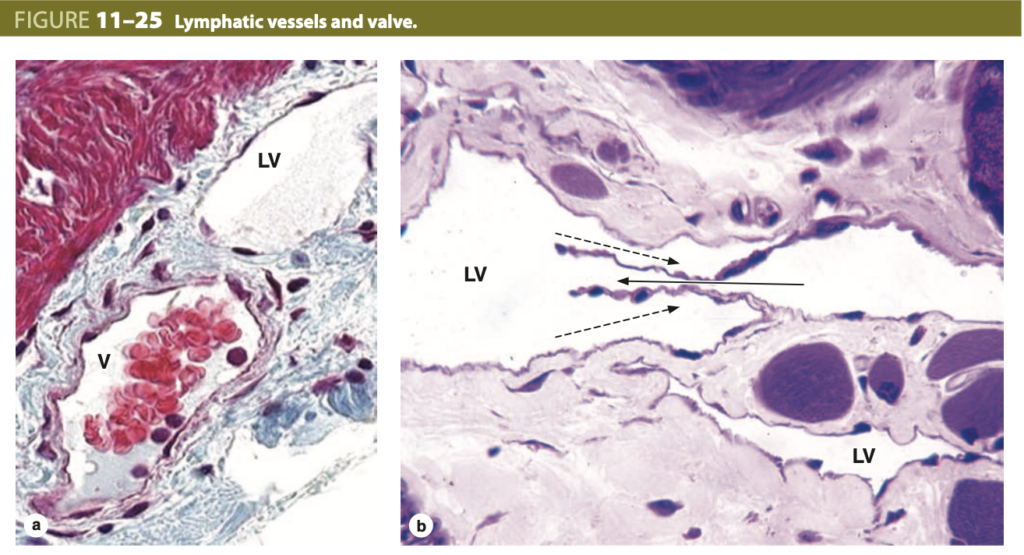
リンパ管の構造 (Structure of Lymphatic Vessels)
リンパ毛細血管の合流によってリンパ管が形成されますが、それらの壁は非常に薄いままです。
(a) 横断切片には、小静脈 (venule, V) 近くのリンパ管 (lymphatic vessel, LV) が示されており、壁が厚い小静脈と比較されています。リンパ管には通常、赤血球が含まれていないため、小静脈と区別されます。(X200; Mallory trichrome)
(b) 筋肉内で切断されたリンパ管 (LV) の縦断切片には、リンパの一方向性の流れを確保するための弁 (valve) が示されています。矢印はリンパの流れの方向を示し、点線の矢印は、弁がリンパの逆流をどのように防ぐかを示しています。下の小さなリンパ管は、内皮のみで構成されたリンパ毛細血管です。(X200; PT)
最終的にリンパ管は2つの大きなリンパ管幹である胸管 (thoracic duct) と右リンパ管 (right lymphatic duct) に収束し、リンパを血液に戻します。胸管は左内頸静脈 (left internal jugular vein) と左鎖骨下静脈 (left subclavian vein) の合流点付近で血管系に接続し、右リンパ管は右鎖骨下静脈 (right subclavian vein) と右内頸静脈 (right internal jugular vein) の合流点付近で血液循環系に流入します。これらの最も大きなリンパ管の構造は、小静脈 (small veins) に類似しており、外膜 (adventitia) は比較的未発達ですが、栄養血管 (vasa vasorum) と神経ネットワークが含まれています。
リンパ系血管は間質液をリンパとして収集し、血液に戻すだけでなく、リンパ球 (lymphocytes)、抗体 (antibodies)、および他の免疫成分を運搬し、多くの臓器やリンパ節 (lymph nodes)、その他のリンパ組織 (lymphoid tissues) へと分配する重要な役割を果たします。
医学的応用 (Medical Application)
リンパ管および大きなリンパ管は、病原体 (pathogens)、寄生虫 (parasites)、悪性細胞 (malignant cells) が体内に拡散するのを促進するため、臨床的に重要です。リンパ節の外科的除去は、がんの転移の有無を確認するための標準的な手順ですが、リンパの排出を妨げ、影響を受けた部位の組織に腫れやリンパ浮腫 (lymphedema) を引き起こす可能性があります。
循環系のまとめ
心臓 (Heart)
- 心臓には3つの主要な層があります:
(1) 内皮 (endothelium) と基底膜下の結合組織から成る内膜 (endocardium)、
(2) 心筋 (cardiac muscle) から成る中膜 (myocardium)、
(3) 多くの脂肪細胞 (adipocytes) を含む結合組織と中皮 (mesothelium) で覆われた外膜 (epicardium) です。 - 心臓の伝導系 (cardiac conducting system) は規則的な収縮を刺激し、修飾された心筋線維で構成される洞房結節 (SA node) と房室結節 (AV node)、房室束 (bundle of His)、左および右の脚 (bundle branches)、プルキンエ線維 (Purkinje fibers) から成ります。
- プルキンエ線維は、両心室の内膜下層 (subendocardial layer) に位置し、収縮性の心筋線維よりも直径が大きく、グリコーゲンが豊富で、筋原線維 (myofibrils) の束はまばらです。
- 密な不規則結合組織 (dense irregular connective tissue) から成る心臓骨格 (cardiac skeleton) は、すべての心臓弁の基部を囲み、心房と心室を分離し、心筋の挿入部を提供します。
血管系 (Vasculature)
- 肉眼で見える血管には、3つの主要な層、またはチュニック (tunics) があります:(1) 内膜 (intima) は内皮、結合組織、および大きな血管では内弾性板 (internal elastic lamina) を含みます。(2) 中膜 (media) は平滑筋とコラーゲンまたは弾性板が交互に層をなしています。(3) 外膜 (adventitia, または外層) は結合組織、栄養血管 (vasa vasorum)、および神経 (nerves) を含みます。
- 血管を通じて、内皮細胞は単なる心臓や血管のライナーではなく、血液凝固を防ぐ因子や、隣接する平滑筋細胞を収縮または弛緩させる因子、損傷や感染部位で炎症を引き起こす因子を積極的に生成します。
- 動脈は、サイズや壁の構成によって分類されます:(1) 大動脈などの弾性動脈 (elastic arteries) は、厚い中膜に多数のフェネストレーションを持つ弾性板を含みます。(2) 筋性動脈 (muscular arteries) は中型の動脈です。(3) 小動脈 (small arteries) は中膜に10層未満の平滑筋があります。
- 微小血管系 (Microvasculature) は、外科的操作が不可能なほど小さく、ほとんどの臓器に浸透しており、次の構造から成ります:(1) 1~3層の平滑筋からなる細動脈 (arterioles)、(2) 内皮層 (endothelial layer) のみで構成される毛細血管 (capillaries)、(3) 大きなルーメン (lumen) と薄い壁を持ち、毛細血管の排出を行う小静脈 (venules)。
- 終末細動脈 (Terminal arterioles) は前毛細血管 (metarterioles) に分岐し、ここで平滑筋の括約筋が血流を抑制するために収縮し、脈動的に血液が毛細血管床に流れ、周囲の細胞との間で代謝交換が行われます。
- 毛細血管 (Capillaries) は、分子や細胞の交換に応じて異なる程度の透過性を持つ3つの構造的および機能的タイプに分類されます:(1) 多数のタイトジャンクションを持つ連続性毛細血管 (continuous capillaries) では、すべての交換が細胞を通じて行われます。(2) 細胞内に小さな穴やフェネストレーションを持つ有窓性毛細血管 (fenestrated capillaries)。(3) より大きなルーメンを持ち、内皮細胞の間に大きな隙間があり、基底膜が不連続な洞様毛細血管 (discontinuous capillaries)、または洞 (sinusoids)。
- 毛細血管床 (capillary beds) は通常、小静脈 (venules) に排出され、これは微小血管系の最後のセグメントです。後毛細血管小静脈 (postcapillary venules) は、白血球 (white blood cells) が損傷または感染した組織に侵入する場所です。
- 連続性毛細血管 (continuous capillaries) および後毛細血管小静脈 (postcapillary venules) の内皮は、周皮細胞 (pericytes) と呼ばれる薄い細胞によって取り囲まれており、その収縮が血流を助け、微小血管系のリモデリング (remodeling) や修復の際には平滑筋および結合組織に変化することができます。
- 2つの代替的な微小血管経路には、動静脈吻合 (arteriovenous anastomoses)、またはAVシャント (AV shunts) があり、ここでは細動脈が毛細血管床を迂回できます。また、静脈門脈系 (venous portal systems) では、毛細血管床から排出された小静脈が再び分岐し、別の毛細血管床を形成します。
- 小静脈、中型静脈、大静脈はすべて、壁の厚さを超えるルーメン径を持ち、心臓に血液を戻します。内膜の弁 (intimal valves) は逆流を防ぎ、発達したチュニック (tunics) を持つようになります。
リンパ管 (Lymphatic Vessels)
- 静脈に引き込まれなかった間質液 (interstitial fluid) は、リンパ (lymph) として盲端のリンパ管 (lymphatics) に排出され、これらは非常に薄い内皮細胞 (endothelial cells) の壁を持ち、細胞間に空間があります。
- リンパ管は、薄壁のリンパ管に収束し、リンパは周囲の筋肉や臓器の動きによって推進され、内膜の弁が流れを一方向に保ちます。
- 最大のリンパ管である胸管 (thoracic duct) と右リンパ管 (right lymphatic duct) は、どちらも静脈と類似した層構造を持つ壁を持ち、心臓付近の静脈に合流してリンパを循環系に戻します。


コメント