Contents
呼吸不全—病態生理、診断、酸素療法
多くの呼吸器疾患の診断と治療は、呼吸とガス交換の基本的な生理学的原則を理解することに大きく依存しています。呼吸不全(respiratory insufficiency)は、換気の不十分さから生じることもあれば、肺膜を通る拡散の異常や、肺と組織間のガス輸送の異常から生じることもあります。これらの疾患に対する治療法はしばしば異なるため、単に「呼吸不全」と診断するだけでは不十分です。
呼吸異常を学ぶための有用な方法
前の章では、肺活量(vital capacity)、潮気(tidal air)、機能的残気量(functional residual capacity)、死腔(dead space)、生理的シャント(physiologic shunt)、生理的死腔(physiological dead space)などの測定方法について説明しました。これらの測定は臨床肺生理学者(clinical pulmonary physiologist)の道具の一部に過ぎません。他にもいくつかのツールがあります。
血液ガスと血液pHの測定
肺機能の基本的な検査として、血液中の酸素(O₂)の分圧(Po₂)、二酸化炭素(CO₂)、およびpHの測定があります。急性呼吸困難(acute respiratory distress)や酸塩基平衡(acid–base balance)の急性異常を診断するためには、これらの測定を迅速に行うことが重要です。以下に示す簡単で迅速な方法は、数滴の血液で数分以内にこれらの測定を行うために開発されています。
血液pHの測定
血液pHは、化学実験室で一般的に使用されるガラスpH電極(glass pH electrode)を用いて測定されますが、ここで使用される電極は小型化されています。ガラス電極が生成する電圧はpHの直接的な測定値であり、通常はボルテメーター(voltmeter)のスケールで直接読み取られるか、チャートに記録されます。
血液CO₂の測定
血液CO₂の測定にもガラス電極pHメーターが使用されます。CO₂ガスが弱い炭酸水素ナトリウム(sodium bicarbonate)溶液に曝露されると、CO₂は溶液中に溶解し、平衡状態に達します。この平衡状態において、溶液のpHはCO₂と炭酸水素イオン(bicarbonate ion, HCO₃⁻)の濃度に依存し、ヘンダーソン-ハッセルバルヒ方程式(Henderson-Hasselbalch equation)に従います(Chapter 31で説明):
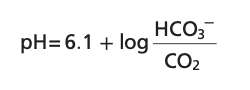
ガラス電極を使用して血液中のCO₂を測定する場合、小型のガラス電極が薄いプラスチック膜(plastic membrane)で囲まれています。電極とプラスチック膜の間に、既知の濃度の炭酸水素ナトリウム溶液(sodium bicarbonate solution)が置かれ、血液がプラスチック膜の外側に超過します。これにより、CO₂が血液から炭酸水素ナトリウム溶液に拡散します。血液はわずか数滴で済みます。その後、ガラス電極でpHを測定し、以前に示された式を使用してCO₂を計算します。
血液Po₂の測定
液体中の酸素(O₂)の濃度は、ポラログラフィー(polarography)と呼ばれる技術を使用して測定できます。電流が小さな負の電極と溶液の間で流され、電極の電圧が溶液の電圧と−0.6ボルト以上異なると、O₂が電極に沈着します。さらに、電極を通る電流の流れの速度はO₂の濃度(したがって、PO₂にも)に直接比例します。実際には、表面積が約1平方ミリメートルの負のプラチナ電極(negative platinum electrode)が使用され、この電極は薄いプラスチック膜で血液から隔てられています。この膜はO₂の拡散は許可しますが、電極を「中毒」させるようなタンパク質や他の物質の拡散は許可しません。
しばしば、pH、CO₂、Po₂の測定装置は同一の装置に組み込まれており、1滴の血液でこれらの測定を数分以内に行うことができます。これにより、血液ガスレベルとpHの変化をほぼ瞬時にベッドサイドで追跡することができます。
最大呼気流量の測定
多くの呼吸器疾患、特に喘息(asthma)では、呼気時の気流抵抗が非常に大きくなり、呼吸困難を引き起こすことがあります。この状態は「最大呼気流量(maximum expiratory flow)」という概念につながります。最大呼気流量は、次のように定義されます。人が強く呼気を行うと、呼気の流れは最大流量に達し、それ以上に強く息を吐いても流れは増加しません。最大呼気流量は、肺が大きな空気量で満たされているときに、ほぼ空に近いときよりもずっと大きくなります。この原理は図43-1を参照することで理解できます。
図43-1の説明
- 図43-1A では、肺胞(alveoli)と気道(air passageways)の外側に圧力がかかると、胸郭を圧迫することによってその影響が示されています。矢印は、同じ圧力が肺胞と細気管支(bronchioles)を圧迫することを示しています。この圧力は、肺胞から細気管支への空気の移動を促進しますが、同時に細気管支の圧迫も引き起こし、空気の外部への移動を妨げます。細気管支がほぼ完全に閉じると、さらに呼気の力を強めても肺胞内圧は大きくなりますが、細気管支の閉塞と気道抵抗も同じ程度に増加し、流量の増加が阻止されます。したがって、一定の呼気力を超えると、最大呼気流量に達します。
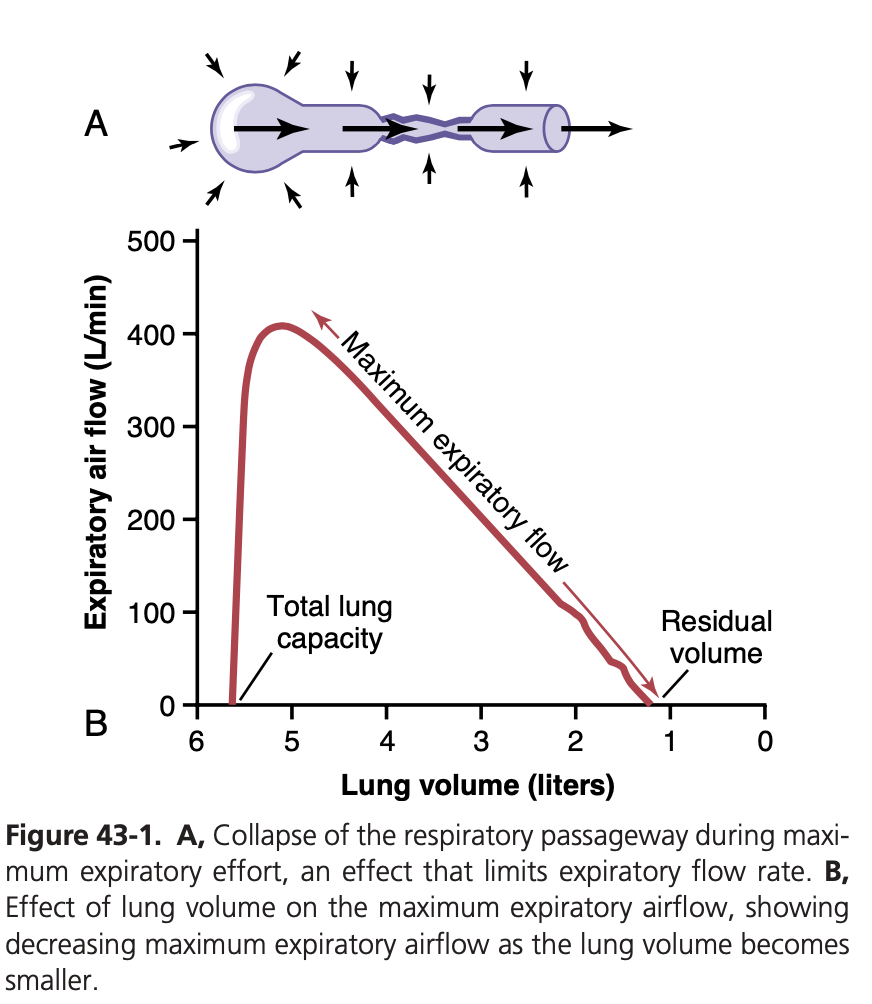
- 図43-1B では、異なる肺の閉塞度(lung collapse)の度合いが最大呼気流量に与える影響が示されています。この図は、健康な人ができるだけ空気を吸い込んでから、最大呼気努力で息を吐き続けると、最大呼気流量がすぐに400 L/minを超えることを示しています。しかし、追加の呼気努力をしても、この流量が超えることはありません。また、肺容量が小さくなると、最大呼気流量も減少します。これは、肺が拡張すると気管支や細気管支が肺の構造要素によって部分的に保持されるためです。肺が小さくなると、これらの構造が弛緩し、外部の胸圧によって気管支や細気管支がより簡単に閉じるため、最大呼気流量が減少します。
最大呼気流量-容量曲線の異常
- 図43-2 では、正常な最大呼気流量-容量曲線と、2種類の肺疾患(狭窄肺(constricted lungs)と部分的気道閉塞(partial airway obstruction))における流量-容量曲線が示されています。狭窄肺では、全肺活量(TLC)と残気量(RV)が減少します。また、肺が最大容量に拡張できないため、最大呼気流量は正常な曲線と同じレベルには達しません。狭窄肺疾患には、結核(tuberculosis)、珪肺(silicosis)、胸郭の狭窄(kyphosis, scoliosis)、線維性胸膜炎(fibrotic pleurisy)などがあります。
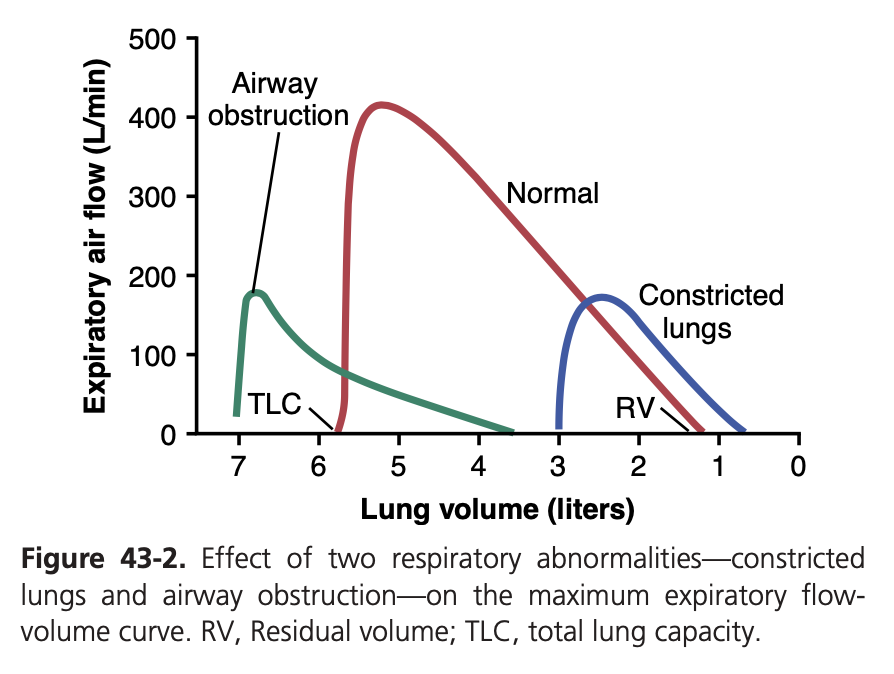
- 気道閉塞のある疾患では、呼気が吸気よりも難しくなります。これは、呼気時に胸に追加の正圧が必要となるため、気道の閉塞傾向が大きく増加するからです。対照的に、吸気時の追加の負圧が気道を開けるため、空気が肺に入りやすくなりますが、肺内に閉じ込められやすくなります。長期間にわたると、この影響でTLCとRVが増加し(図43-2の緑の曲線)、気道の閉塞により最大呼気流量が大きく減少します。気道閉塞を引き起こす典型的な疾患は喘息(asthma)であり、重度の気道閉塞は一部の肺気腫(emphysema)の段階でも見られます。
強制呼気肺活量(Forced Expiratory Vital Capacity, FVC)と強制呼気量(Forced Expiratory Volume, FEV1)
もう一つの有用な臨床検査は、スパイロメーター(spirometer)で記録された強制呼気肺活量(FVC)です。図43-3Aは正常な肺のFVC、図43-3Bは部分的な気道閉塞のある人のFVCを示しています。FVCマニューバー(maneuver)を行うと、まず最大限に吸気してTLCに達し、その後できるだけ速く完全に呼気します。肺容量記録の下り斜面の全距離がFVCを示します。
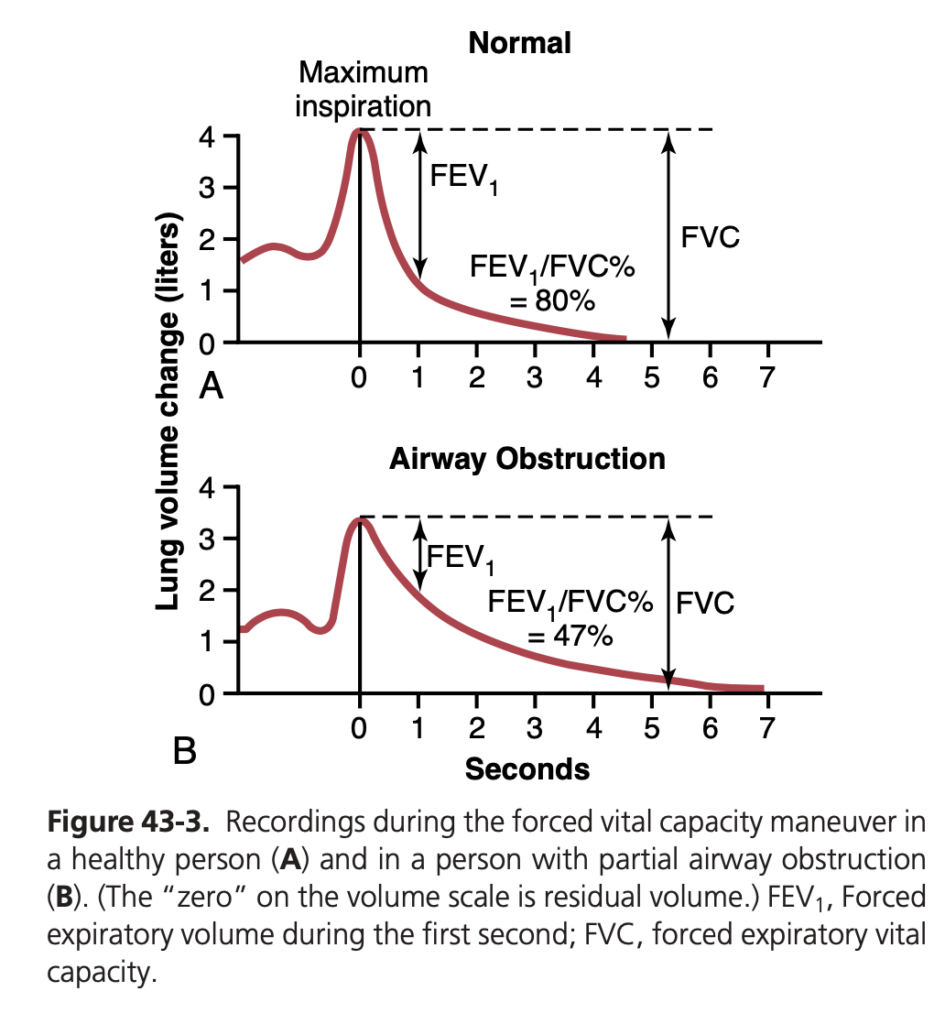
正常な肺と部分的な気道閉塞の記録の違いを比較すると、FVCの全体的な容量変化は大きく異ならず、基本的な肺容量における違いは中程度です。しかし、特に最初の1秒間における呼気量の差が大きいです。したがって、最初の1秒間の強制呼気量(FEV1)を正常値と比較するのが一般的です。正常な人では(図43-3A参照)、1秒間に呼気されるFVCの割合(FEV1/FVC%)は80%です。しかし、気道閉塞がある場合(図43-3B参照)では、この値は47%に低下します。重度の気道閉塞では、急性喘息などでこの値が20%以下に減少することもあります。
特定の肺疾患の病態生理
慢性肺気腫(Chronic Pulmonary Emphysema)
慢性肺気腫(chronic pulmonary emphysema)とは、文字通り「肺内の過剰な空気」を意味しますが、この用語は通常、長年の喫煙によって引き起こされる複雑な閉塞性および破壊的な肺のプロセスを表すために使われます。肺での主要な病態生理的変化は以下の通りです。
- 慢性感染(Chronic Infection): 喫煙やその他の刺激物質の吸入によって気管支(bronchi)や細気管支(bronchioles)が慢性的に感染します。この感染は気道の正常な防御機構を大きく乱し、たとえばニコチン(nicotine)によって呼吸上皮(respiratory epithelium)の線毛(cilia)が部分的に麻痺します。その結果、粘液(mucus)が気道から容易に排出できなくなります。さらに、過剰な粘液分泌が刺激され、状態が悪化します。また、肺胞マクロファージ(alveolar macrophages)が抑制され、感染との戦いが効果的でなくなります。
- 気道の慢性閉塞(Chronic Obstruction of Airways): 感染、過剰な粘液、そして細気管支上皮(bronchiolar epithelium)の炎症性浮腫(inflammatory edema)が、細気管支の多くで慢性的な閉塞を引き起こします。
- 肺胞の破壊(Destruction of Alveoli): 気道の閉塞は特に呼気時に困難を引き起こし、これにより肺胞内に空気が閉じ込められ、肺胞が過度に伸展します。この影響と肺の感染が組み合わさり、肺胞壁の50%から80%が著しく破壊されます。最終的な肺気腫の図は、図43-4(上)および43-5に示されています。
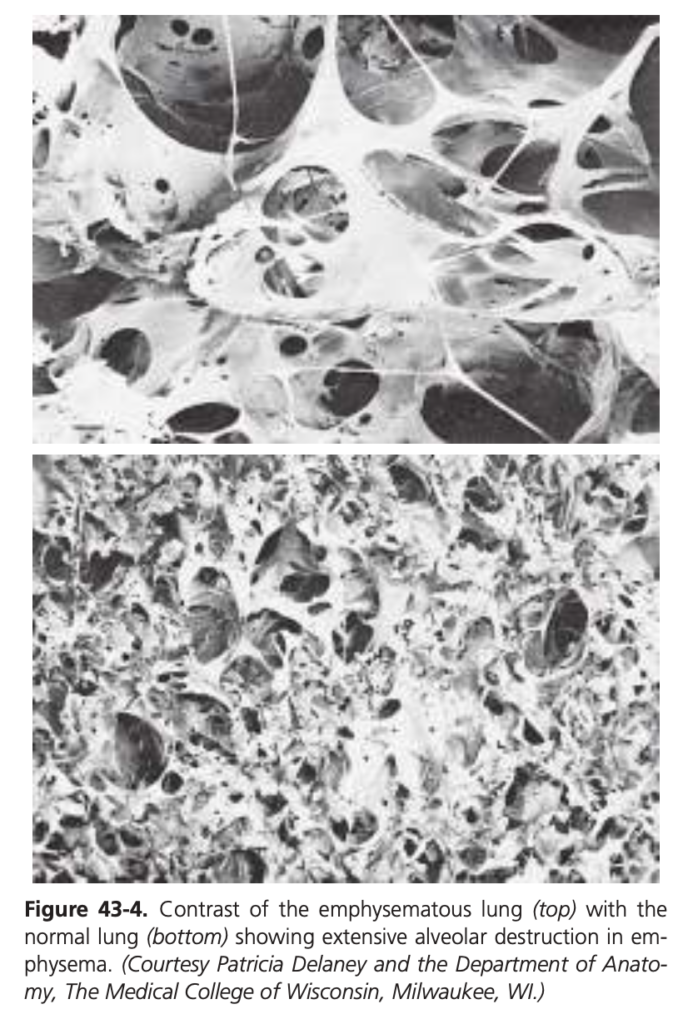
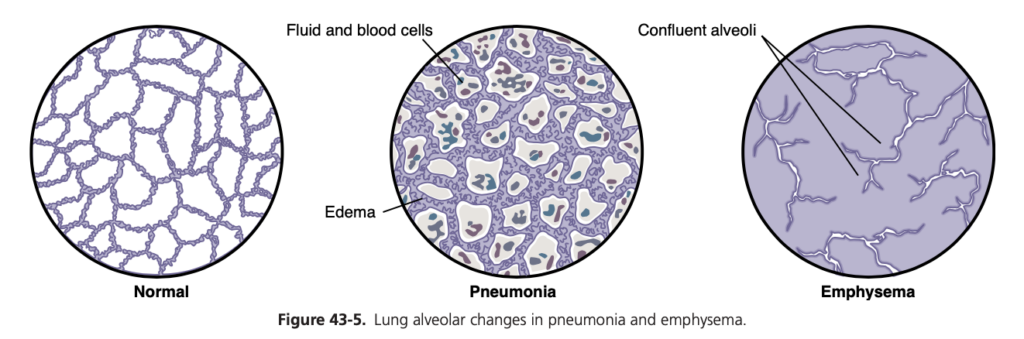
慢性肺気腫の生理的影響
慢性肺気腫の生理的影響は、疾患の重症度や気管支閉塞と肺実質(lung parenchyma)の破壊の程度によって異なります。以下の異常が見られます:
- 気道抵抗の増加(Increased Airway Resistance): 気道の閉塞は気道抵抗を増加させ、呼吸の労力が大幅に増加します。呼気時には気管支が圧迫されるため、気道を通過する空気が非常に難しくなり、気道抵抗がさらに増加します。
- 肺の拡散能の低下(Decreased Diffusing Capacity): 肺胞壁の著しい損失により、肺の拡散能が大幅に低下します。これにより、血液を酸素化する能力と二酸化炭素(CO2)を血液から除去する能力が低下します。
- 異常な換気-灌流比(Abnormal Ventilation-Perfusion Ratios): 閉塞プロセスが肺の一部では非常に悪化し、他の部分では比較的良好であるため、肺の一部が良好に換気され、他の部分が不十分に換気される状況が生じます。この状況は、非常に低い換気-灌流比(V_A/Q)を持つ部位(生理的シャント(physiological shunt))と、非常に高い換気-灌流比を持つ部位(生理的死腔(physiological dead space))が同じ肺内に存在し、血液の換気が不十分になることがあります。
- 肺血管抵抗の増加(Increased Pulmonary Vascular Resistance): 大部分の肺胞壁の損失も肺内の毛細血管の数を減少させます。その結果、肺血管抵抗が大幅に増加し、肺高血圧(pulmonary hypertension)が発生し、右心系に負担がかかり、右心不全(right-sided heart failure)を引き起こすことがあります。
慢性肺気腫は通常、何年にもわたって徐々に進行します。多くの肺胞の低換気と肺胞壁の損失によって、低酸素症(hypoxia)と高二酸化炭素血症(hypercapnia)が発生します。これらの影響の結果として、長期間にわたる激しい呼吸困難が続き、最終的に低酸素症と高二酸化炭素血症が死を引き起こすことがあります。これは喫煙の高い代償です。
肺炎(Pneumonia)
肺炎(pneumonia)とは、肺の炎症状態であり、肺胞が液体や血液細胞で満たされることを含みます(図43-5参照)。一般的な肺炎のタイプは細菌性肺炎(bacterial pneumonia)で、最も頻繁に肺炎球菌(pneumococci)によって引き起こされます。この病気は肺胞での感染から始まり、肺膜が炎症を起こし、非常に多くの液体や赤血球および白血球が血液から肺胞に漏れ出します。その結果、感染した肺胞は液体や細胞で徐々に満たされ、感染が肺胞から肺胞へと広がります。最終的には、肺の大部分、時には全葉または全肺が「固化(consolidated)」し、液体や細胞残骸で満たされます。
肺炎の人では、肺のガス交換機能が疾患の異なる段階で低下します。初期段階では、肺炎のプロセスが片方の肺に局所化していることがあり、肺胞換気が減少する一方で、血液の流れは正常に続きます。この状態は、次の2つの主要な肺の異常を引き起こします:
- 呼吸膜の総表面積の減少(Reduction in Total Respiratory Membrane Surface Area)
- 換気-灌流比の低下(Decreased Ventilation-Perfusion Ratio)
これらの影響により、低酸素血症(hypoxemia)と高二酸化炭素血症(hypercapnia)が生じます。
- 図43-6 では、肺炎における換気-灌流比の低下の影響が示されています。換気されている肺を通過する血液は97%の酸素飽和度を示しますが、換気されていない肺を通過する血液は約60%の酸素飽和度を示します。その結果、左心から大動脈に送られる血液の平均酸素飽和度は約78%であり、正常値を大きく下回ります。
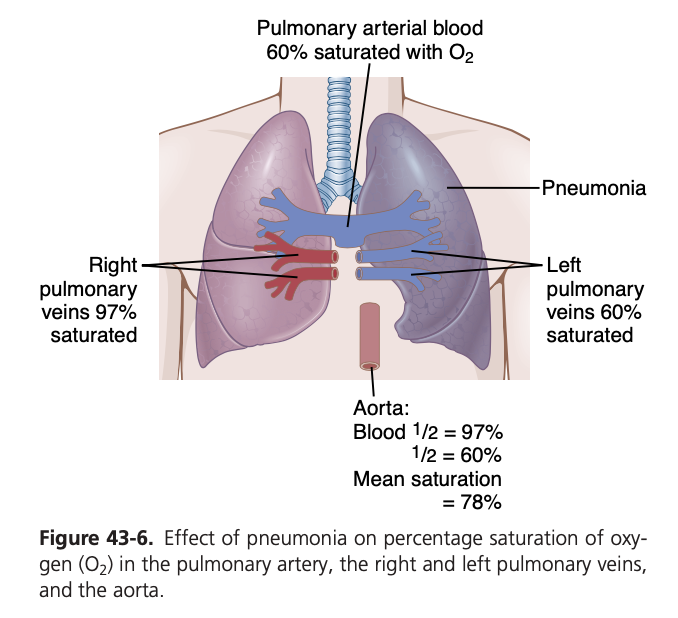
特定の肺疾患の病態生理
虚脱(Atelectasis)
虚脱(atelectasis)とは、肺胞の虚脱を意味し、局所的な肺の部分や全肺にわたって発生する可能性があります。虚脱の一般的な原因は次の2つです:
- 気道閉塞(Airway Obstruction):
- 粘液による小気管支の閉塞(Blockage of Small Bronchi with Mucus): 粘液が多くの小気管支を塞ぎます。大きな粘液プラグまたは固体物体(Blockage by a Large Mucous Plug or Solid Object): 大きな粘液プラグや腫瘍などが主要な気管支を閉塞します。
- 虚脱による全体的な肺機能への影響(Effects on Overall Pulmonary Function): 全肺の虚脱は、肺胞の閉塞だけでなく、虚脱した肺の血管の抵抗を増加させます。これは、肺の体積の減少によって血管が圧迫されるためです。また、虚脱した肺の酸素不足(hypoxia)が追加の血管収縮(vasoconstriction)を引き起こします。結果として、虚脱した肺を通る血流は大幅に減少し、ほとんどの血液は換気されている肺を通ります。図43-7では、5/6の血液が換気された肺を通過し、1/6が非換気肺を通過します。これにより、全体的な換気-灌流比(ventilation-perfusion ratio)は中程度に損なわれ、動脈血の酸素飽和度は軽度に低下します。
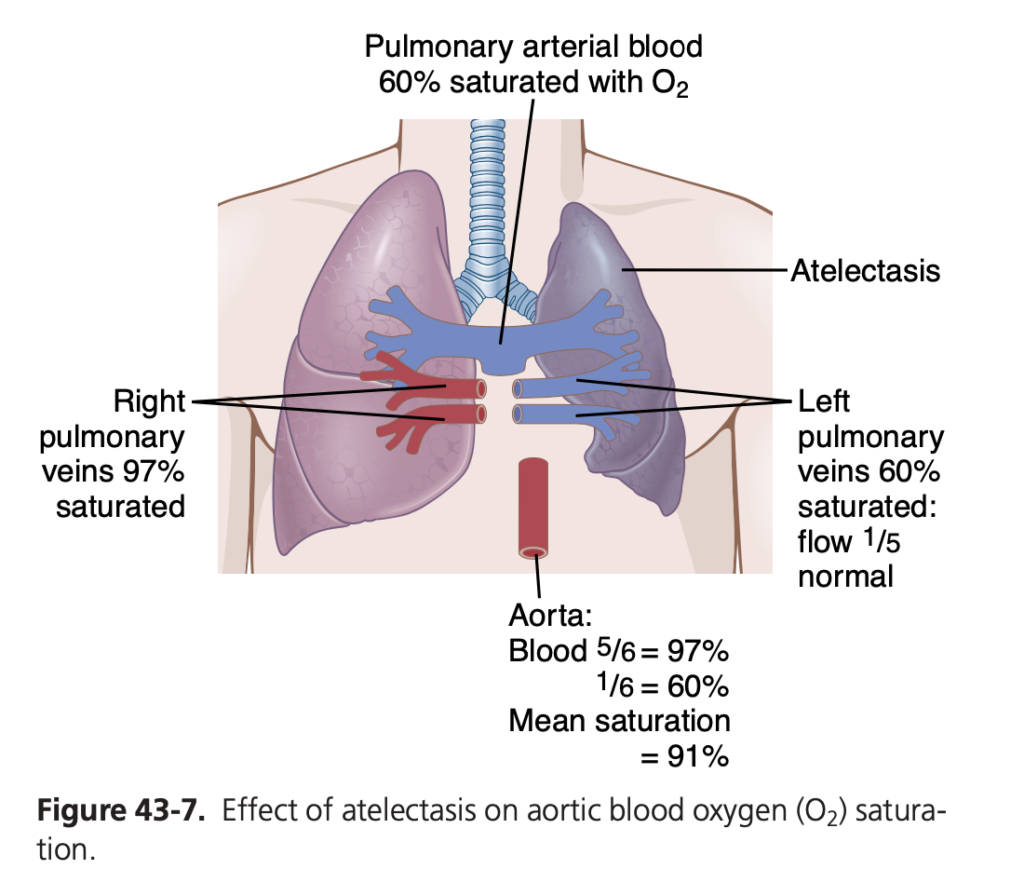
- サーファクタントの欠乏(Lack of Surfactant):
- サーファクタントの役割(Role of Surfactant): サーファクタントは、肺胞を覆う液体中に分泌され、肺胞内の表面張力を2倍から10倍に低下させることで肺胞の虚脱を防ぎます。
- サーファクタント欠乏症(Surfactant Deficiency): ハイアリン膜疾患(hyaline membrane disease)や呼吸窮迫症候群(respiratory distress syndrome)などでは、サーファクタントの分泌が大幅に減少し、肺胞の表面張力が正常よりも何倍も高くなります。このサーファクタント欠乏が肺の虚脱または液体で満たされる原因となり、多くの新生児が窒息で死亡することがあります。
喘息(Asthma)
喘息(asthma)は、気管支の平滑筋が痙攣して部分的に閉塞を引き起こし、極度の呼吸困難をもたらします。喘息の原因は以下の通りです:
- アレルギー性過敏反応(Allergic Hypersensitivity): 30歳未満の患者の約70%が、植物花粉などに対するアレルギーによって喘息を発症します。
- 非アレルギー性過敏反応(Non-Allergic Hypersensitivity): 高齢者では、スモッグなどの非アレルゲンに対する過敏反応が原因となります。
喘息では、免疫グロブリンE(IgE)抗体が過剰に産生され、これが気管支周辺の肥満細胞(mast cells)に付着します。アレルゲンがIgE抗体と反応すると、以下の物質が放出されます:
- ヒスタミン(Histamine)
- アナフィラキシスの遅延反応物質(Slow-Reacting Substance of Anaphylaxis)
- 好酸球化学誘引因子(Eosinophilic Chemotactic Factor)
- ブラジキニン(Bradykinin)
これらの物質は、気管支の壁に局所的な浮腫を引き起こし、気管支内に粘液を分泌し、平滑筋の痙攣を引き起こします。これにより気道抵抗が大幅に増加し、特に呼気時に気道が圧迫されるため、喘息患者は吸気は比較的容易でも、呼気に困難を感じます。
- 喘息発作中の肺機能の変化(Changes in Lung Function during Asthma Attack): 発作中には、肺の機能残気量(functional residual capacity)と残気量(residual volume)が特に増加します。長期的には胸郭が永久に拡大し、バレルチェスト(barrel chest)が形成され、機能残気量と肺の残気量が恒常的に増加します。
結核(Tuberculosis)
結核(tuberculosis)では、結核菌(tubercle bacilli)が肺で特有の組織反応を引き起こします:
- マクロファージによる侵入(Invasion by Macrophages): 感染した組織にマクロファージが侵入します。
- 結核の形成(Formation of Tubercle): 繊維組織によって病変が「壁で囲まれる」ことで結核が形成されます。このプロセスは、感染の拡張を防ぐ保護的な過程です。
治療が行われない場合、結核菌は肺内に広がり、肺組織の大規模な破壊と大きな膿瘍の形成を引き起こします。遅期の結核は次の特徴があります:
- 呼吸筋の仕事の増加(Increased Work of Respiratory Muscles): 呼吸筋にかかる負担が増し、肺の換気や肺活量が低下します。
- 呼吸膜の表面積の減少(Reduced Respiratory Membrane Surface Area): 呼吸膜の厚さが増し、肺の拡散能が低下します。
- 異常な換気-灌流比(Abnormal Ventilation-Perfusion Ratio): これにより、O2とCO2の肺の拡散がさらに低下します。
低酸素症(Hypoxia)と酸素療法(Oxygen Therapy)
低酸素症(hypoxia)とは、体内の細胞が十分な酸素を得られない状態です。酸素療法は、低酸素症の種類によって効果が異なります。以下に、低酸素症の分類と酸素療法の効果について説明します。
低酸素症の分類
- 外因性の原因による血液の酸素化不良(Inadequate Oxygenation of Blood in the Lungs due to Extrinsic Reasons):
- 大気中の酸素不足(Deficiency of O2 in the Atmosphere): 高高度などで酸素濃度が低下することによる。
- 換気不良(Hypoventilation): 神経筋疾患などによる換気の低下。
- 肺疾患(Pulmonary Disease):
- 気道抵抗の増加または肺のコンプライアンスの低下による換気不良(Hypoventilation due to Increased Airway Resistance or Decreased Pulmonary Compliance): 気道が狭くなり、換気が不十分になる。
- 異常な肺胞換気-灌流比(Abnormal Alveolar Ventilation-Perfusion Ratio): 生理的死腔の増加や生理的シャントの増加などが含まれます。
- 呼吸膜の拡散能力の低下(Diminished Respiratory Membrane Diffusion): 肺胞から血液への酸素拡散が減少します。
- 静脈-動脈シャント(Venous-to-Arterial Shunts):
- 右から左への心臓シャント(右-左シャント)により、酸素化されていない血液が動脈系に送られることによる。
- 血液による酸素輸送の不良(Inadequate O2 Transport to the Tissues by the Blood):
- 貧血または異常なヘモグロビン(Anemia or Abnormal Hemoglobin): 酸素運搬能力が低下します。
- 全体的な循環不良(General Circulatory Deficiency): 循環全体の不足。
- 局所的循環不良(Localized Circulatory Deficiency): 周辺、脳、冠状動脈などでの循環不良。
- 組織浮腫(Tissue Edema): 組織に液体が溜まり、酸素の供給が妨げられます。
- 組織の酸素利用能力の不良(Inadequate Tissue Capability of Using O2):
- 細胞酸化酵素の中毒(Poisoning of Cellular Oxidation Enzymes): シアナイド中毒などで、酸素が利用できない状態。
- 細胞の代謝能力の低下(Diminished Cellular Metabolic Capacity): ビタミン欠乏などで酸素利用が低下する状態。
酸素療法の効果
酸素療法の効果は、低酸素症の種類によって異なります。
- 大気中の酸素不足(Atmospheric Hypoxia):
- 酸素療法により、吸入する酸素の濃度が100%になり、酸素レベルを完全に回復させることができます。
- 換気不良(Hypoventilation):
- 100%酸素を吸入することで、1回の呼吸で肺胞に移動する酸素量が通常の5倍になります。しかし、二酸化炭素(CO2)については効果がありません。
- 肺胞膜の拡散障害(Impaired Alveolar Membrane Diffusion):
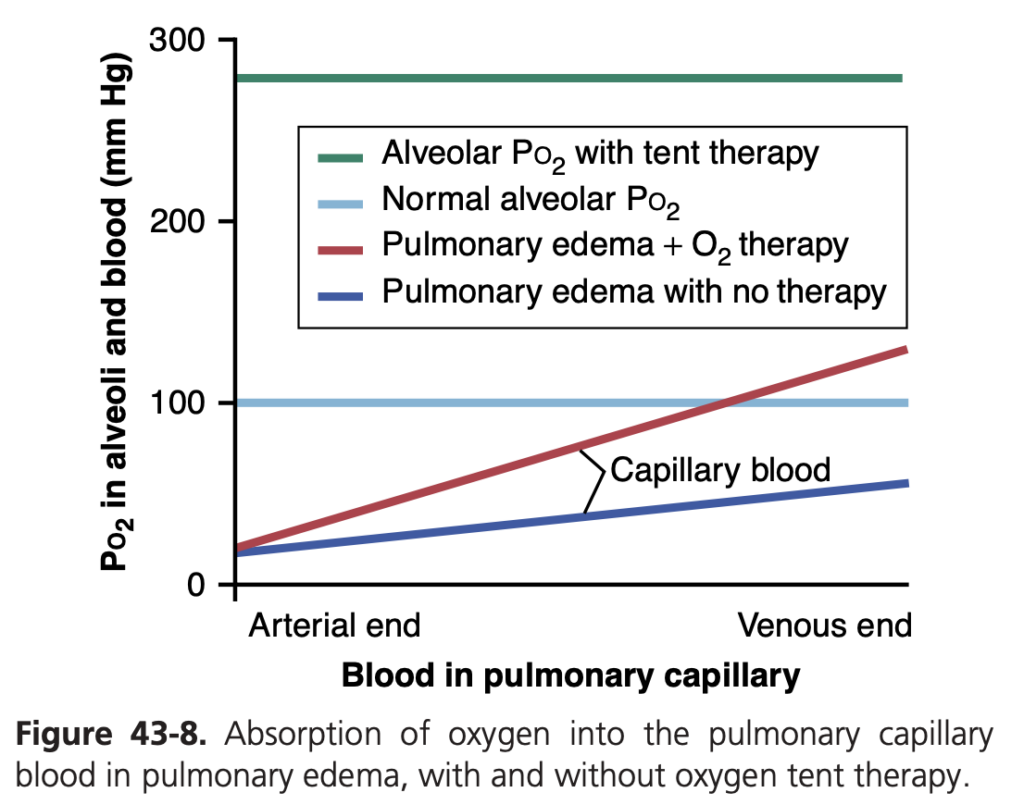
- 酸素療法により、肺胞内の酸素分圧(Po2)が約100 mm Hgから600 mm Hgに増加します。これにより、酸素の拡散圧勾配が大幅に増加し、酸素の取り込みが促進されます。これにより、肺水腫などで酸素の取り込みが3〜4倍速くなることが示されています。
- 貧血、異常ヘモグロビン輸送、循環不良、または生理的シャント(Anemia, Abnormal Hemoglobin Transport, Circulatory Deficiency, or Physiological Shunt):
- 酸素療法の効果は限られており、肺胞の酸素量が最大であっても、酸素輸送の問題が解決されない場合があります。ただし、肺胞内の酸素が最大になることで、血液中に溶解した酸素がわずかに増加することがあり、これが生死を分けることがあります。
- 組織の酸素利用能力の不良(Inadequate Tissue Use of O2):
- 酸素療法は有効ではありません。酸素の取り込みや輸送に異常がない場合、酸素療法では組織での酸素利用能力は改善されません。
チアノーシス(Cyanosis)
チアノーシス(cyanosis)とは、皮膚が青紫色に変わる状態で、皮膚の血管、特に毛細血管に酸素が不足したヘモグロビンが過剰に存在することによります。酸素が欠乏したヘモグロビンは、強い暗青紫色を持ち、それが皮膚を通して見えるためです。
- 定義と閾値(Threshold for Cyanosis):
- 動脈血中に100 mlあたり5グラム以上の脱酸素ヘモグロビンが含まれると、チアノーシスが明確に現れます。
- 貧血のある人は、ヘモグロビンが少ないためにチアノーシスが現れることはほとんどありません。一方、多血症(polycythemia vera)などでヘモグロビンが過剰に存在する場合、通常の状態でもチアノーシスが見られることがあります。
高炭酸ガス血症(Hypercapnia)—体液中の二酸化炭素の過剰
高炭酸ガス血症(hypercapnia)は、体内の二酸化炭素(CO2)が過剰になる状態で、以下のように分類されます。
高炭酸ガス血症の発生条件
- 換気不足(Hypoventilation):
- 酸素と二酸化炭素の移動の影響: 換気が不十分だと、肺胞内での酸素と二酸化炭素の交換が影響を受けます。換気が減少することで、酸素の取り込みが減少し、二酸化炭素の排出も減少します。その結果、高炭酸ガス血症と低酸素症(hypoxia)が同時に発生することがあります。
- 循環不良(Circulatory Deficiency):
- 二酸化炭素の除去の減少: 血液の循環が不十分な場合、組織から二酸化炭素の除去が減少し、組織内に二酸化炭素が蓄積します。血液の二酸化炭素運搬能力は酸素の3倍以上ですが、組織内の高炭酸ガス血症は低酸素症ほど深刻ではありません。
- 他の低酸素症の原因:
- 大気中の酸素不足、ヘモグロビンの不足、酸化酵素の中毒: これらの原因では、酸素の供給や利用に関する問題があるため、高炭酸ガス血症は通常発生しません。
- 肺胞膜を通じた拡散障害: 二酸化炭素は酸素よりも20倍速く拡散するため、通常、高炭酸ガス血症は発生せず、もし発生しても、肺の換気が刺激されて解消されます。
高炭酸ガス血症の症状と影響
- 軽度から重度の症状:
- 軽度: 肺胞内の二酸化炭素圧(Pco2)が60~75 mm Hgを超えると、通常の呼吸の深さと頻度では満足できなくなり、呼吸困難(dyspnea)がひどくなります。
- 中度から重度: Pco2が80~100 mm Hgに達すると、無気力(lethargic)や半昏睡状態(semicomatose)になることがあります。Pco2が120~150 mm Hgに達すると、呼吸が抑制され、最終的に呼吸停止(respiratory death)に至る可能性があります。
呼吸困難(Dyspnea)
呼吸困難(dyspnea)とは、十分な換気が得られないことによる精神的苦痛のことです。一般的には「空気飢餓(air hunger)」と呼ばれます。
- 呼吸困難の要因:
- 体液中の呼吸ガスの異常(Abnormality of Respiratory Gases): 特に高炭酸ガス血症と少しの低酸素症。
- 呼吸筋の仕事量(Work of Respiratory Muscles): 十分な換気を維持するために必要な労力。
- 精神状態(State of Mind): 恐怖や不安などが呼吸困難を増幅させることがあります。
- 呼吸困難の発生例:
- 二酸化炭素の蓄積: 二酸化炭素が過剰に蓄積すると呼吸困難が生じます。
- 正常なガスレベルでの強い呼吸: 二酸化炭素と酸素が正常でも、強い呼吸を維持することで呼吸困難を感じることがあります。
- 神経性呼吸困難(Neurogenic Dyspnea): 呼吸機能や体液中のガスが正常でも、心理的な要因で呼吸困難を感じることがあります。
人工呼吸(Artificial Respiration)
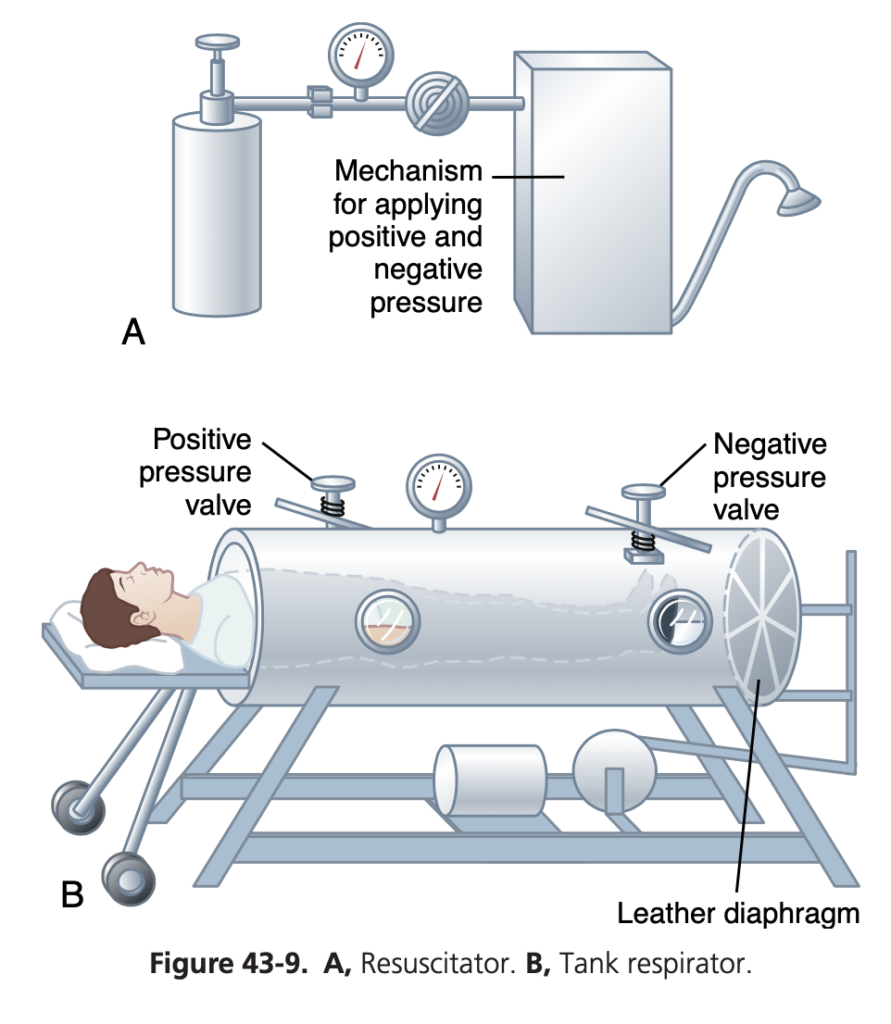
- レスキュー装置(Resuscitator):
- 基本的な構造: 酸素または空気の供給タンク、間欠的陽圧機構、マスクまたは気管内チューブ接続部などで構成され、呼吸を補助します。現在の装置は調整可能な陽圧制限を持ち、正常な肺には12〜15 cm H2Oの圧力が設定されることが一般的です。
- タンク式呼吸器(Iron Lung):
- 構造と機能: 患者の体がタンク内に入り、頭部だけが外に出る構造です。タンク内の圧力を変化させることで、呼吸を助けます。現在では、より優れた機械的換気装置が使用されることが一般的です。
- 人工呼吸器とタンク式呼吸器の血行への影響:
- 高圧の影響: 高圧での人工呼吸やタンク式呼吸器の使用は、心臓への血流を阻害し、心臓出力を低下させることがあります。特に30 mm Hgを超える圧力は危険で、長時間の使用は致命的になる可能性があります。


コメント