Contents
- 1 目的
- 2 拡散電位 (Diffusion Potential) と膜電位 (Membrane Potential) の概要
- 3 イオン濃度による膜電位
- 4 ナーンズト電位 (Nernst Potential)
- 5 ゴールドマン方程式 (Goldman Equation) または ゴールドマン・ホジキン・カッツ方程式 (Goldman-Hodgkin-Katz Equation)
- 6 ニューロンの静止膜電位 (Resting Membrane Potential of Neurons) – 約−90ミリボルト
- 7 ニューロンのアクションポテンシャル (Neuron Action Potential)
- 8 アクションポテンシャルの開始 (Initiation of the Action Potential)
- 9 アクションポテンシャルの伝播 (Propagation of the Action Potential)
- 10 一部のアクションポテンシャルにおけるプラトー (Plateau in Some Action Potentials)
- 11 一部の興奮性組織のリズム性—反復的放電 (Rhythmicity of Some Excitable Tissues—Repetitive Discharge)
- 12 神経幹における信号伝達の特別な特徴 (Special Characteristics of Signal Transmission in Nerve Trunks)
- 13 「跳躍伝導」 (Saltatory Conduction)
- 14 刺激閾値と「急性局所電位」 (Threshold for Excitation and “Acute Local Potentials”)
- 15 不応期 (Refractory Period)
- 16 安定剤と局所麻酔薬 (Stabilizers and Local Anesthetics)
目的
- 拡散電位 (Diffusion Potential), 膜電位 (Membrane Potential), 静止膜電位 (Resting Membrane Potential), 脱分極 (Depolarization), 過分極 (Hyperpolarization), 再分極 (Repolarization) について定義する。
- アクションポテンシャル (Action Potential) がどのように生成されるかを説明する。
- アクションポテンシャルの異なる特性を理解する。
- いくつかの興奮性組織のリズム性 (Rhythmicity) を説明する。
- 跳躍伝導 (Saltatory Conduction) のメカニズムを説明する。
- 神経伝達に影響を与える薬物について知る。
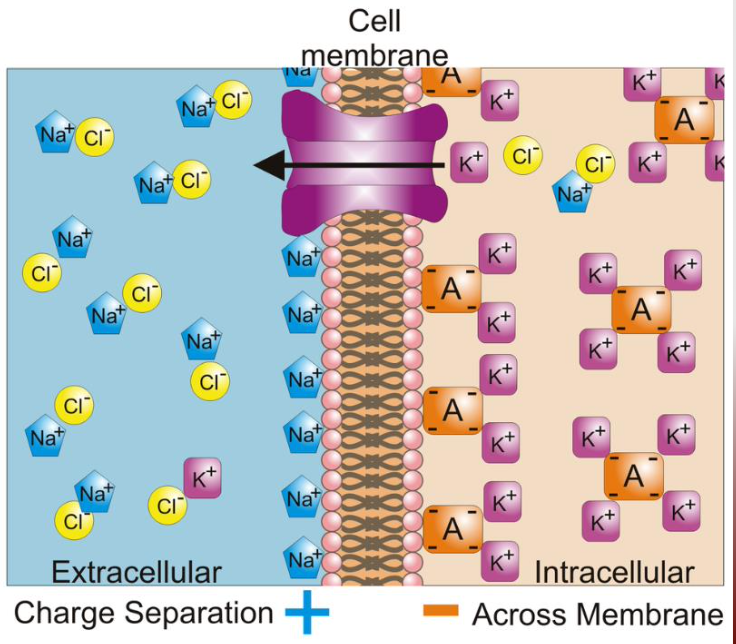
拡散電位 (Diffusion Potential) と膜電位 (Membrane Potential) の概要
拡散電位 (Diffusion Potential)
拡散電位は、細胞膜を横切るイオンの移動によって生じる電位差です。具体的には、あるイオンが膜を越えて移動し、そのイオンの濃度勾配が膜内外で異なるとき、電位差が生じます。この電位差が大きくなると、イオンのさらなる移動を防ぐことができます。例えば、カリウムイオン (Potassium ion) の場合、細胞内の電位が外部より約94ミリボルト (mV) 負に帯びています。
膜電位 (Membrane Potential)
膜電位は、膜の内外でのイオンの分布により生じる電位勾配です。ポジティブなイオンは膜の「ネガティブな」側に引き寄せられ、ネガティブなイオンは「ポジティブな」側に引き寄せられます。これにより、イオンは受動的に一方向に移動します。
イオン濃度による膜電位
カリウムイオン (Potassium Ion)
正常な哺乳動物の神経繊維におけるカリウムイオンの膜電位は、細胞内が約94ミリボルト (mV) 負に帯びています。
ナトリウムイオン (Sodium Ion)
ナトリウムイオンの場合、膜電位は細胞内が約61ミリボルト (mV) 正に帯びています。
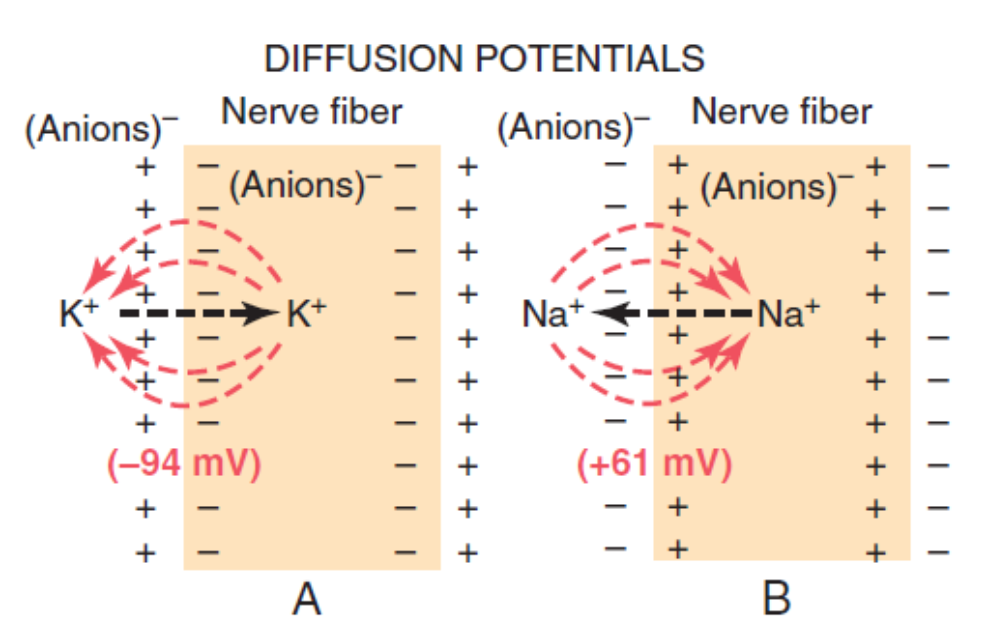
ナーンズト電位 (Nernst Potential)
ナーンズト電位 (Nernst Potential)
特定のイオンについて、膜を横切る拡散電位であり、そのイオンの膜を通過するネット拡散を正確に防ぐ電位です。これは、その特定のイオンの膜の両側の濃度比によって決まります。濃度比が大きいほど、イオンが一方向に拡散する傾向が強く、さらなるネット拡散を防ぐために必要なナーンズト電位も大きくなります。
ゴールドマン方程式 (Goldman Equation) または ゴールドマン・ホジキン・カッツ方程式 (Goldman-Hodgkin-Katz Equation)
ゴールドマン方程式 (Goldman Equation)
細胞膜が複数の異なるイオンに対して透過性を持つ場合、膜電位の計算には次の3つの要因が関係します:
- イオンの電荷の極性 (Polarity of the Electrical Charge of Each Ion)
各イオンの電荷が膜電位に与える影響を考慮します。 - 膜の透過性 (Permeability of the Membrane, P) 各イオンに対する膜の透過性が膜電位を決定する要因となります。
- イオンの濃度 (Concentrations, C) 膜の内側 (i) と外側 (o) のイオン濃度の比率が膜電位に影響を与えます。
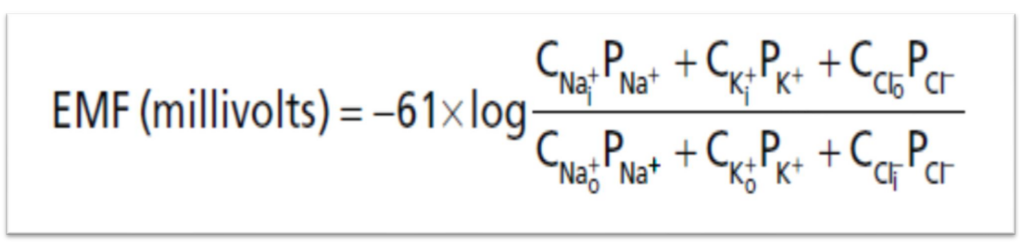
ゴールドマン方程式は、ナトリウムイオン (Na+)、カリウムイオン (K+)、および塩素イオン (Cl−) の3種類のイオンが関与する場合に、膜内側の計算された膜電位を示します。
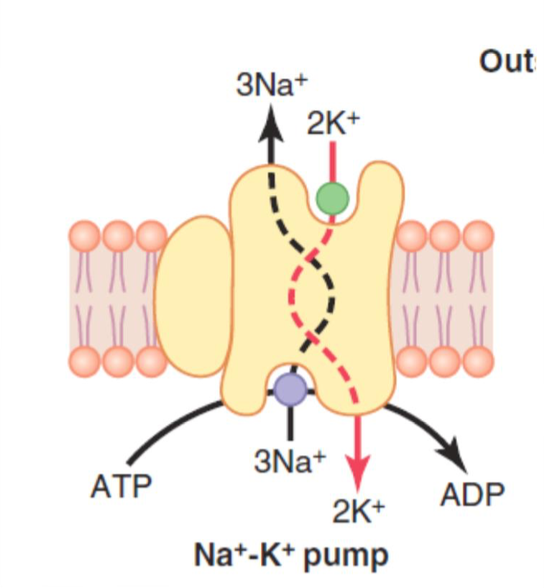
ニューロンの静止膜電位 (Resting Membrane Potential of Neurons) – 約−90ミリボルト
ナトリウム-カリウムポンプ (Sodium-Potassium Pump, Na+-K+ Pump)
ナトリウム-カリウムポンプは電気生成型ポンプ (Electrogenic Pump) です。このポンプは、内側に比べて外側に多くの正の電荷を排出します。その結果、内側には正のイオンが不足し、膜電位が負の値になります。
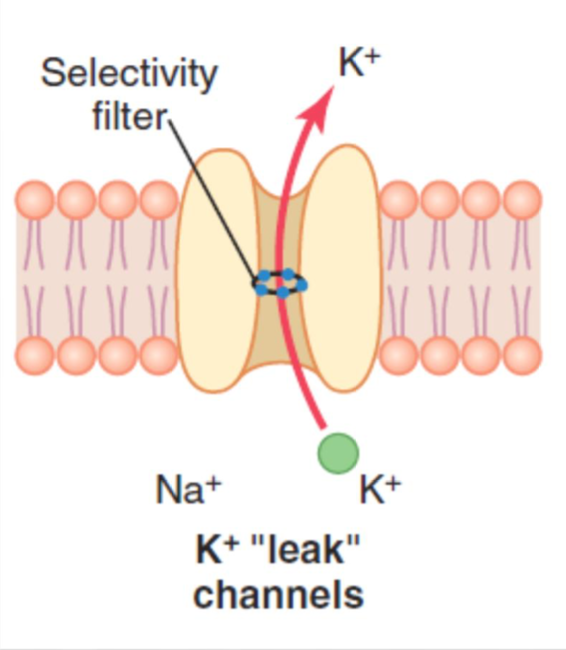
タンデムポアドメインカリウムチャネル (Tandem Pore Domain Potassium Channel) またはカリウム「リーク」チャネル (Potassium Leak Channel)
カリウムイオン (K+) は、静止状態でも細胞膜を通過することができます。このチャネルはナトリウムイオン (Na+) に対してもわずかに透過性がありますが、カリウムに対してはるかに透過性が高いです。これが、通常の静止膜電位のレベルを決定する主要な要因です。
ニューロンのアクションポテンシャル (Neuron Action Potential)
アクションポテンシャル (Action Potentials)
アクションポテンシャルは、神経繊維膜に沿って急速に広がる膜電位の変化です。これには、通常の静止膜電位から急激に正の電位への変化があり、その後、ほぼ同じ速さで負の電位に戻ります。神経信号を伝導するためには、アクションポテンシャルが神経繊維に沿って伝播し、繊維の端に到達します。
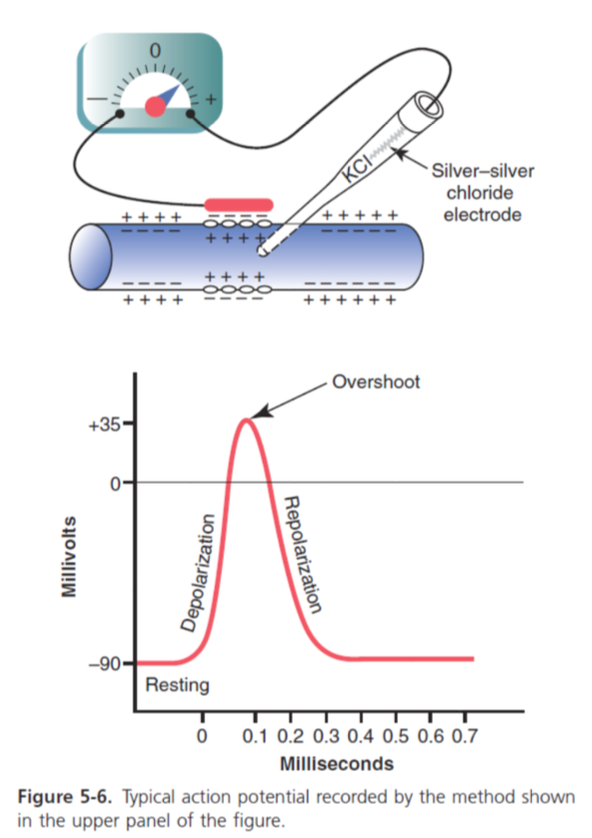
静止期 (Resting Stage)
静止膜電位 (Resting Membrane Potential)
アクションポテンシャルが始まる前の膜電位を指します。この状態では膜が「偏極 (Polarized)」していると言います。これは、膜内側が−90ミリボルト (mV) の負の電位を持っているためです。
脱分極期 (Depolarization Stage)
脱分極 (Depolarization)
膜が突然ナトリウムイオン (Sodium Ions) に対して透過性を持つようになります。これにより、大量の正の電荷を持つナトリウムイオンが軸索 (Axon) の内部に拡散します。膜電位は急速に正の方向に上昇します。
- 大きな神経繊維の場合 (Large Nerve Fibers): 大量のナトリウムイオンの流入により、膜電位がゼロレベルを超えて一時的に正の状態になります。
- 小さな神経繊維や中枢神経系のニューロン (CNS Neurons): 膜電位はゼロレベルに近づくだけで、正の状態にはならないことが多いです。
再分極期 (Repolarization Stage)
再分極 (Repolarization)
数十万分の一秒以内にナトリウムチャネル (Sodium Channels) が閉じ始め、カリウムチャネル (Potassium Channels) が通常よりも大きく開きます。これにより、カリウムイオンが急速に細胞外へ拡散し、通常の負の静止膜電位が再び確立されます。
アクションポテンシャルの開始 (Initiation of the Action Potential)
ポジティブフィードバックサイクル (Positive-Feedback Cycle) によるナトリウムチャネルの開放
アクションポテンシャルの開始には、膜電位の初期上昇が十分に大きくなり、ナトリウムチャネルが開くための正のフィードバックサイクルが必要です。
- 閾値 (Threshold for Initiation): アクションポテンシャルが発生するには、膜電位が15〜30ミリボルト (mV) ほど急激に上昇する必要があります。大きな神経繊維では、膜電位が−90ミリボルト (mV) から−65ミリボルト (mV) まで上昇すると、アクションポテンシャルが爆発的に発生します。
- −65ミリボルト (mV) が刺激の閾値です。
アクションポテンシャルの伝播 (Propagation of the Action Potential)
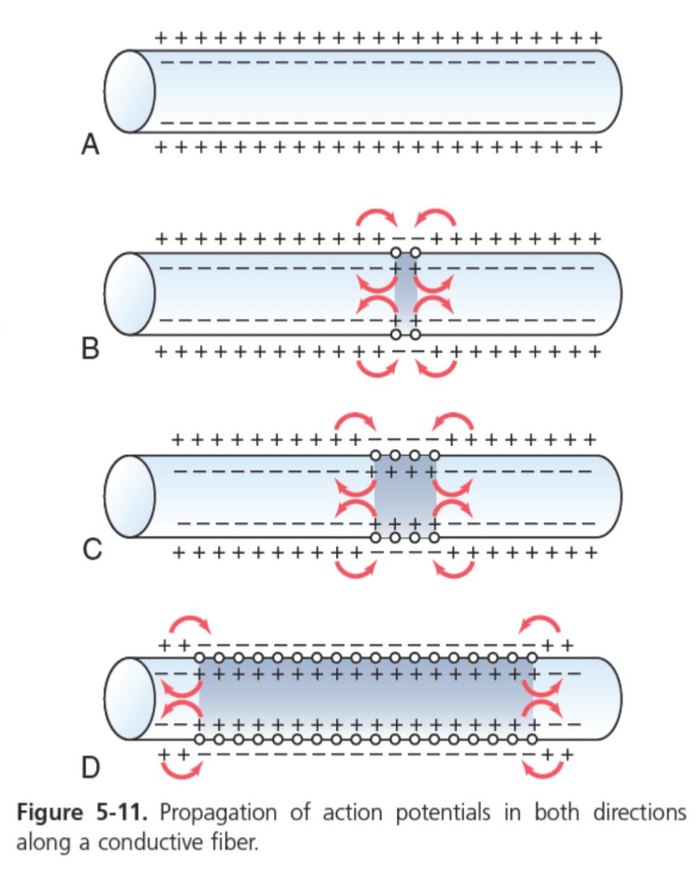
伝播の方向 (Direction of Propagation)
興奮性膜 (Excitable Membrane) は、特定の一方向にのみ伝播するわけではありません。アクションポテンシャルは刺激から全ての方向に伝わり、神経繊維の全ての分岐に沿って移動します。これにより、膜全体が脱分極 (Depolarization) するまで、アクションポテンシャルが広がります。
全か無かの法則 (All-or-Nothing Principle)
脱分極の過程は、条件が整っていれば膜全体に広がりますが、条件が整っていない場合は全く伝わりません。膜の特定の点で、次の膜領域を刺激してインパルス (Impulse) の伝播を継続するための十分な電圧が生成されない場合、伝播は停止します。アクションポテンシャルが発生する閾値 (Threshold for Excitation) に対する比率は、常に1以上でなければならず、これが伝播の安全係数 (Safety Factor for Propagation) です。
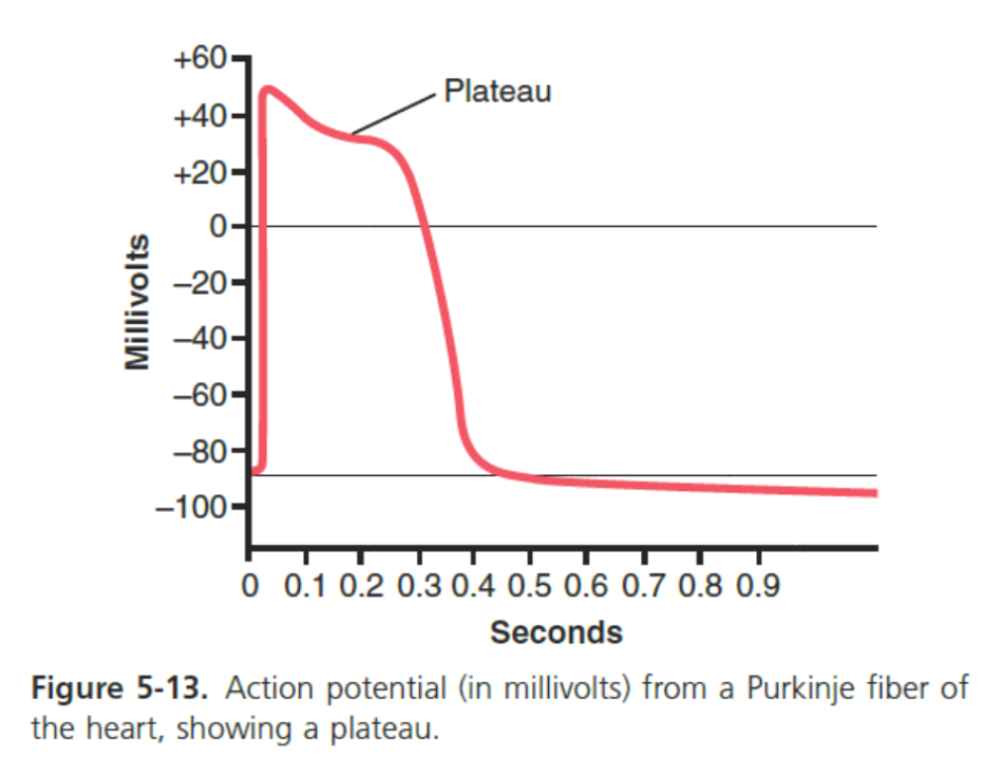
一部のアクションポテンシャルにおけるプラトー (Plateau in Some Action Potentials)
プラトー (Plateau)
プラトーは脱分極期間を大幅に延長します。このタイプのアクションポテンシャルは心筋 (Heart Muscle) の繊維で発生し、プラトーは0.2〜0.3秒続きます。これにより、心筋の収縮も同じ長期間続くことになります。
原因 (Causes):
心筋では、脱分極過程に2つのタイプのチャネルが関与します:
- 通常の電位依存性ナトリウムチャネル (Voltage-Activated Sodium Channels, Fast Channels)
これがアクションポテンシャルのスパイク (Spike) 部分を引き起こします。 - 電位依存性カルシウム-ナトリウムチャネル (Voltage-Activated Calcium-Sodium Channels, L-Type Calcium Channels, Slow Channels)
これらは開くのが遅く、カルシウムイオン (Calcium Ions) が繊維内に入ることを可能にし、プラトー部分を主に担当します。
第2の要因:
電位依存性カリウムチャネル (Voltage-Gated Potassium Channels) は、通常よりも遅れて開きます。これにより、プラトーが終了するまで膜電位が元の−80〜−90ミリボルト (mV) の負の値に戻るのが遅れます。プラトーはカルシウム-ナトリウムチャネルが閉じ、カリウムイオンの透過性が増加した時に終了します。
一部の興奮性組織のリズム性—反復的放電 (Rhythmicity of Some Excitable Tissues—Repetitive Discharge)
反復的自己誘発放電 (Repetitive Self-Induced Discharges)
この現象は心臓 (Heart)、多くの平滑筋 (Smooth Muscle)、および中枢神経系 (CNS) の多くのニューロン (Neurons) で見られます。この現象の原因は以下の通りです:
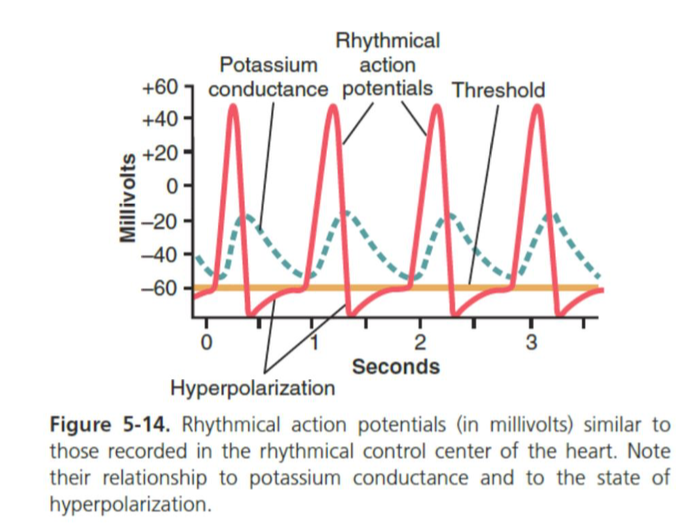
- 心臓のリズミカルな拍動 (Rhythmical Beat of the Heart)
- 腸のリズミカルな蠕動運動 (Rhythmical Peristalsis of the Intestines)
- 呼吸のリズミカルな制御 (Rhythmical Control of Breathing) に関連するニューロンの活動
膜透過性と脱分極 (Membrane Permeability and Depolarization)
心臓のリズムを制御する中心 (Rhythmical Control Center) の「静止」膜電位 (Resting Membrane Potential) は、−60から−70ミリボルト (mV) しかなく、ナトリウムイオン (Sodium Ions) やカルシウム-ナトリウムチャネル (Calcium-Sodium Channels) を完全に閉じるには十分な負の電圧ではありません。したがって、膜はナトリウムイオンやカルシウムとナトリウムイオンが通過できるほど透過性を持つ必要があります。この透過性があることで、膜の自動的な脱分極が可能になります。
以下の順序でプロセスが進行します:
- ナトリウムイオンとカルシウムイオンの一部が内側に流入します (Some Sodium and Calcium Ions Flow Inward)。
- 膜電位が正の方向に増加し、膜の透過性がさらに増加します (Increases the Membrane Voltage in the Positive Direction)。
- さらに多くのイオンが内側に流入し (More Ions Flow Inward)、透過性がさらに増加します。
- このプロセスが繰り返され、最終的にアクションポテンシャル (Action Potential) が生成されます。
アクションポテンシャルの終わりに、膜は再分極 (Repolarization) します。その後、数ミリ秒から数秒の遅延の後、再び自発的な興奮性が生じて脱分極が発生し、新たなアクションポテンシャルが自発的に発生します。このサイクルは繰り返され、興奮性組織の自己誘発リズム性興奮 (Self-Induced Rhythmical Excitation) を引き起こします。
過分極 (Hyperpolarization)
これは、アクションポテンシャルの終わりごろに発生し、その後短期間続きます。この期間中、膜はカリウムイオン (Potassium Ions) に対してより透過性が高くなります。これにより、膜の外側に大量の正の電荷が移動し、繊維内側には通常よりもかなり多くの負の電荷が残ります。この状態では、自己再興奮 (Self-Re-Excitation) が発生しません。その後、カリウム伝導性 (Potassium Conductance) が増加し、過分極状態は徐々に消失します。これにより、膜電位が再び閾値 (Threshold) まで増加し、興奮が可能になります。
神経幹における信号伝達の特別な特徴 (Special Characteristics of Signal Transmission in Nerve Trunks)
神経幹の構成 (Composition of Nerve Trunks)
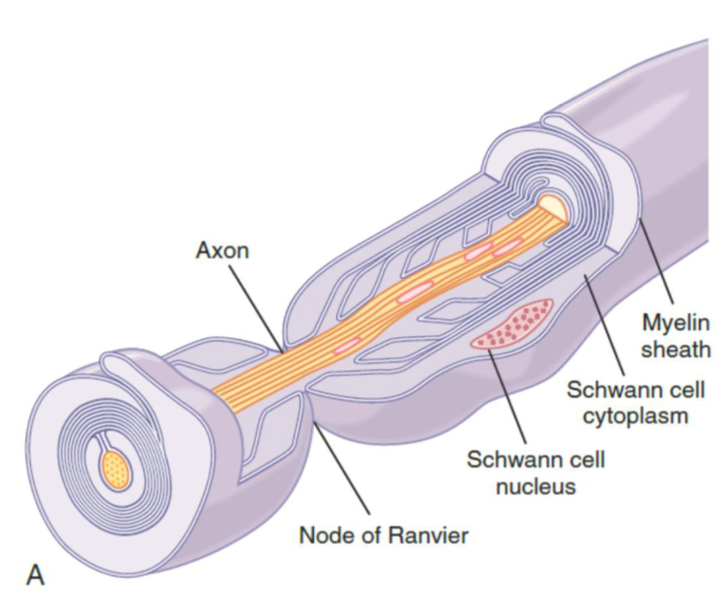
通常、神経幹 (Nerve Trunk) には、髄鞘を持たない無髄線維 (Unmyelinated Fibers) が髄鞘を持つ有髄線維 (Myelinated Fibers) の約2倍含まれています。軸索 (Axon) の中心には粘性のある細胞内液 (Viscid Intracellular Fluid) である軸索質 (Axoplasm) が満たされています。また、軸索は髄鞘 (Myelin Sheath) で囲まれており、この髄鞘は軸索自体よりもかなり厚いです。
髄鞘 (Myelin Sheath) の形成
髄鞘はシュワン細胞 (Schwann Cells) によって軸索の周りに堆積されており、スフィンゴミエリン (Sphingomyelin) という脂質成分を含んでいます。スフィンゴミエリンは優れた電気絶縁体 (Electrical Insulator) です。髄鞘の長さに沿って1~3ミリメートルごとにランビエ絞輪 (Node of Ranvier) が存在し、この部分ではイオンが軸索膜を容易に通過できます。
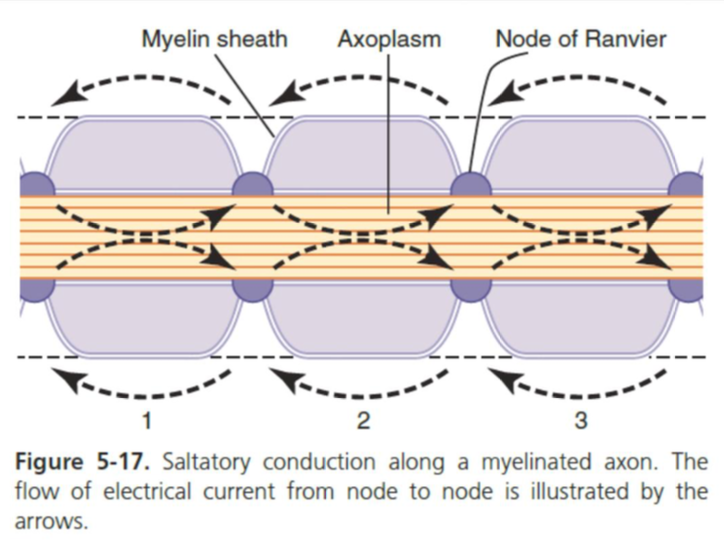
「跳躍伝導」 (Saltatory Conduction)
跳躍伝導の仕組み (Mechanism of Saltatory Conduction)
アクションポテンシャル (Action Potentials) は、ランビエ絞輪からランビエ絞輪へと伝導されます。電流は髄鞘の外側にある周囲の細胞外液 (Extracellular Fluid) を通じて流れ、次々と隣接する絞輪を興奮させます。これにより、神経インパルス (Nerve Impulse) が繊維に沿って跳ぶように伝わります。
跳躍伝導の利点 (Advantages of Saltatory Conduction):
- 神経伝達速度の増加 (Increased Velocity of Nerve Transmission)
有髄線維では、跳躍伝導によって神経伝達速度が5倍から50倍に増加します。 - エネルギーの節約 (Energy Conservation)
跳躍伝導では、脱分極 (Depolarization) がランビエ絞輪だけで発生するため、必要とされるイオンの損失が通常の100分の1程度に抑えられます。また、再分極 (Repolarization) も少ないイオン移動で可能となります。 - アクションポテンシャルの伝導速度 (Velocity of Action Potential Conduction):
無髄線維の小さな繊維では0.25メートル/秒、最大で100メートル/秒の速度で伝導されます。
刺激閾値と「急性局所電位」 (Threshold for Excitation and “Acute Local Potentials”)
弱い刺激と閾値 (Weak Stimulus and Threshold):
弱い負の電気刺激 (Weak Negative Electrical Stimulus) は、繊維を興奮させることができないかもしれませんが、刺激の電圧が増加すると、ある時点で興奮が発生します。
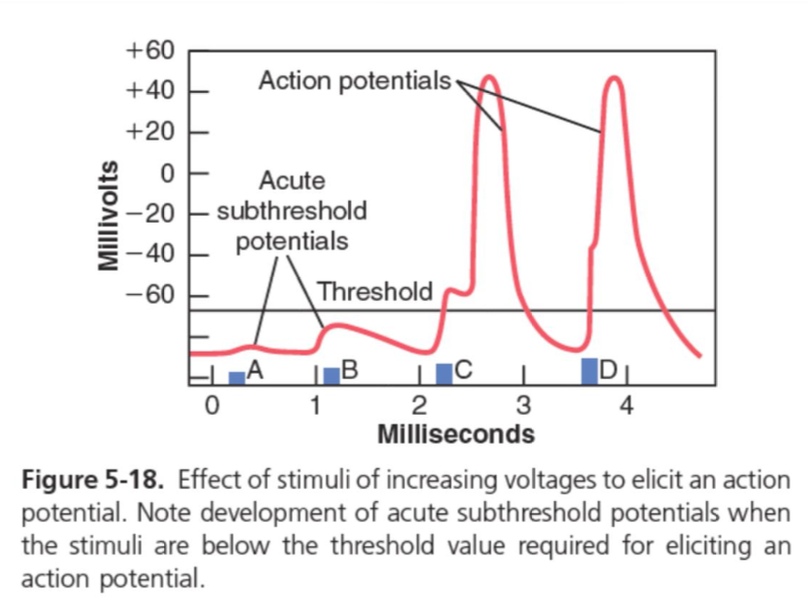
急性局所電位 (Acute Local Potentials):
- ポイントA (Point A):
弱い刺激により膜電位 (Membrane Potential) は−90ミリボルトから−85ミリボルトに変化しますが、この変化はアクションポテンシャル (Action Potential) の自動再生プロセスを発生させるには不十分です。 - ポイントB (Point B):
刺激が強くなるが、それでも強度は十分ではありません。この弱い刺激の後、膜電位は局所的に1ミリ秒以上の間乱れますが、アクションポテンシャルを引き起こすには至りません。これらを急性閾値下電位 (Acute Subthreshold Potentials) と呼びます。 - ポイントC (Point C):
刺激がさらに強くなり、局所電位がアクションポテンシャルを引き起こすための閾値レベル (Threshold Level) に達しますが、発生するまでに短い潜伏期間 (Latent Period) が必要です。 - ポイントD (Point D):
刺激がさらに強くなり、急性局所電位も強くなります。この場合、アクションポテンシャルは潜伏期間がさらに短くなって発生します。
不応期 (Refractory Period)
不応期の仕組み (Mechanism of Refractory Period):
新しいアクションポテンシャルは、膜が前のアクションポテンシャルによってまだ脱分極 (Depolarized) している間は、興奮性繊維 (Excitable Fiber) に発生することはできません。アクションポテンシャルが開始された直後、ナトリウムチャネル (Sodium Channels) やカルシウムチャネル (Calcium Channels) が不活化 (Inactivated) し、この時点でどんな興奮性信号がこれらのチャネルに適用されても、不活化ゲート (Inactivation Gates) は開きません。再び開くためには、膜電位が元の静止膜電位 (Resting Membrane Potential) に戻る必要があります。
絶対不応期 (Absolute Refractory Period):
絶対不応期とは、非常に強い刺激でも2つ目のアクションポテンシャルを引き起こすことができない期間のことです。大きな有髄神経繊維 (Large Myelinated Nerve Fibers) では、約1/2500秒です。
安定剤と局所麻酔薬 (Stabilizers and Local Anesthetics)
膜安定化因子 (Membrane-Stabilizing Factors):
膜の興奮性 (Excitability) を低下させる因子です。例えば、細胞外液 (Extracellular Fluid) 中のカルシウムイオン濃度 (Calcium Ion Concentration) が高いと、膜のナトリウムイオン透過性 (Membrane Permeability to Sodium Ions) が低下し、同時に興奮性も低下します。カルシウムイオンは「安定剤」(Stabilizer) として知られています。
局所麻酔薬 (Local Anesthetics):
例えばプロカイン (Procaine) やテトラカイン (Tetracaine) などは、ナトリウムチャネルの活性化ゲート (Activation Gates of Sodium Channels) に直接作用し、これらのゲートが開きにくくなることで、膜の興奮性が低下します。興奮性が極端に低下すると、アクションポテンシャルの強度と興奮性閾値の比率 (安全率, Safety Factor) が1.0未満になるため、神経インパルスが麻酔された神経を通過することができなくなります。


コメント